Процесът на галванично покритие е един от най-добрите начини за защита от корозия. Методи за галванично покритие
Галванопластика и галванопластика
Електротип- електрохимичен метод на копиране (получаване на точни копия на продуктите). Намира широко приложение в инженерството при производството на матрици в печатарската индустрия, форми за пресоване на плочи и др. Този метод се използва за направата на метални мрежи, бижута, копия на скулптури, гравюри, детайли със сложна конфигурация. Методът се отличава с изключително висока точност на възпроизвеждане на релефа на продукта.
галванопластика- електрохимичен процес на покриване на един метал с друг, по-механично и химически по-стабилен, например стоманените части са покрити с хром, никел; мед - никел, сребро или други метали.
По принцип галваничното покритие не се различава от галваничното. Въпреки това, галванопластичните и галванопластичните процеси имат свои собствени характеристики и се различават преди всичко по методите на подготовка на повърхността преди отлагането на метал върху нея. При галваничното покритие повърхността се подготвя така, че покритието да прилепне здраво към нея. При електроформоването, от друга страна, покритието трябва да може лесно да се отлепи. Ето защо в последния случай се обръща голямо внимание на нанасянето на проводими слоеве (в случай на покритие на непроводници) и на разделителни слоеве (ако копието е получено от метал). Освен това, докато много метали и сплави (сребро, цинк, калай, никел, мед, хром и техните сплави) се използват за галванични покрития, само отлагания на мед, никел и сребро обикновено се използват при галваничното покритие и много по-рядко - други метали . Поради факта, че галванопластичните отлагания се различават от галванопластичните с много по-голяма дебелина, съставите на електролитите и режимите, използвани при галваничното покритие, също се различават донякъде от приетите при галванопластика. При електроформоването металът обикновено се изгражда не върху метал, а върху тънък проводящ слой, отложен върху повърхността на непроводник или върху разделящ, слабо проводим слой, отложен върху метал, следователно, допълнителна операция на "затягане" с металът се въвежда в технологичния процес в сравнение с галваничното покритие - първичното натрупване на метал върху проводящия слой до пълното му затваряне. Съставът на електролитите за бутерни вани и режимът на работа са малко по-различни от обичайните. Оборудването за галванично покритие не се различава от оборудването, използвано за галванично покритие.
Като галванична вана може да се използва всеки стъклен велосипед с такъв размер, че предметът, който ще бъде покрит с метал, може свободно да се постави в него и в същото време да не се приближава твърде близо до анодните плочи. Най-удобно е да използвате четириъгълни стъклени буркани (фиг. 1).
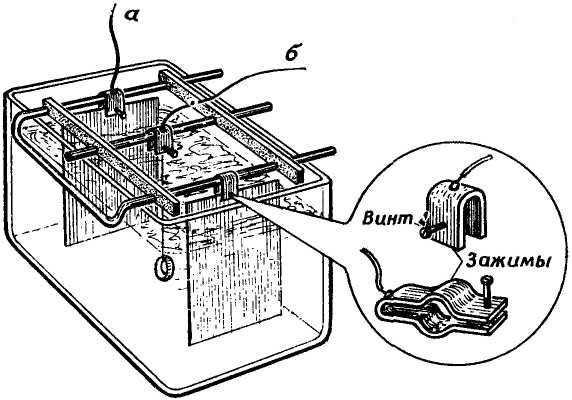
Ориз. 1. Галванична вана в квадратен стъклен буркан.
Напречните пръти се изработват от дебела медна тел или тръби, от които две (а) служат за окачване на никелови или медни пластини - аноди, а третата (б) - за никелирани или медни предмети. В кръгла кутия анодната плоча трябва да бъде огъната под формата на цилиндър (c) (фиг. 2).

Ориз. 2. Галванична вана в кръгъл буркан.
Предметите, които ще бъдат покрити, се окачват на медни проводници. Трябва да има две анодни плочи. Важно е обектите, които ще бъдат покрити, да са обърнати към анодите с най-големите им площи и да са приблизително в успоредни равнини с тях. Напречните греди, от които се окачват анодите и покритите предмети, трябва да бъдат снабдени с клеми за удобно и надеждно свързване (виж фиг. 1). Проводниците, които закрепват анода към напречната греда, трябва да са над нивото на електролита, особено ако са направени от друг метал. Анодните плочи са свързани паралелно една с друга и трябва да бъдат свързани към плюс терминала на източника на ток (батерия или токоизправител).
Анодите трябва да бъдат внимателно почистени от оксиди, мръсотия и мазнини, както и предмети, предназначени за метално покритие. Важно условие за успешното никелиране и медно покритие е чистотата. Ако в електролита се появи лека мътност или се образува утайка, електролитът трябва да се филтрира.

Ориз. 3. Схема на галванична вана.
На фиг. 3 показва схемата на свързване на галваничната вана. Като източник можете да използвате автомобилен акумулатор или токоизправител (напрежение 6-12 V), захранван от мрежа с променлив ток с напрежение 127-220 V. Към веригата трябва да бъдат свързани волтметър и амперметър. Ако повърхността на обекта, който ще бъде покрит, е по-малка от 2 dm 2 , може да се използва милиамперметър 500 mA. Съпротивлението на реостата трябва да бъде от порядъка на 8-10 ома, така че токът да може да се променя в рамките на части от ампер. Когато сглобявате електрическата верига на банята, е много важно да не объркате полюсите на батерията или токоизправителя, тъй като анодните плочи трябва да бъдат свързани към положителния полюс, а частта (обекта) към отрицателния. Ако се включи неправилно, металът на частта или обекта ще се „разтвори“, което ще доведе до влошаване на електролита. Равномерното плътно покритие на обект с никел или мед зависи от големината на електрическия ток, който не надвишава известна граница и зависи от площта на повърхността на обекта. Например, ако скоростта на плътност на тока е 0,5 A на 1 dm 2 и обектът има обща повърхност от около 0,5 dm 2, тогава токът не трябва да надвишава 0,5 x 0,5 \u003d 0,25 A. С по-висок ток, никел или мед ще бъде нанесен в тъмен, крехък, лесно отделящ се слой. Ако обектът има заострени части, плътността на тока трябва да се намали 2-3 пъти. Предметите се потапят във вана под напрежение. За да направите това, те първо се окачват на голи медни проводници с диаметър 0,8-1 mm към напречната греда (медна тръба), свързани към източник на електрически ток (в този случай реостатът се включва за пълно съпротивление) и се спуска във вана с електролит. След това, намалявайки съпротивлението на реостата, доведете тока до нормално. При поцинковане детайлът или предметът се изваждат два-три пъти за кратко време от ваната и се преглеждат. Ако металът е отложен неравномерно, променете позицията на обекта, като го завъртите към анода със страната, от която металният слой е по-тънък.
С правилния процес на никелиране, никелът се отлага в матов, равен, сребрист слой навсякъде. Появата на тъмни петна показва лошо обезмасляване. Тънък слой метал се отлага върху част или обект за 20-30 минути, дебел слой - за няколко часа. Предмет, изваден от ваната, независимо колко добре е бил предварително полиран, има матова повърхност. За придаване на блясък се полира с най-фината креда (прах за зъби) с помощта на кърпа. Можете да полирате и с минзухар, но много внимавайте да не повредите никеловия слой.
Забележка
Алуминият се използва широко в аматьорските дизайни. Може да се направи анодизиране променлив ток 12-24 V. Артикулът (листът) се полира до огледално покритие, избърсва се с ацетон и се обезмаслява химически в разтвор на натриев хидроксид 50 g/l. Време за обезмасляване 3-5 минути, температура на разтвора 50°C. Анодирането с променлив ток е както следва. Ако част (лист) е анодизиран, тогава това е първият електрод, а вторият може да бъде обработена алуминиева заготовка или лист. Контактите на токовите проводници трябва да са алуминиеви. Електролитът е 20% разтвор на сярна киселина.
Условията за анодиране са както следва:
1. За алуминий и плакиран дуралуминий плътността на тока е 1,5-2 A / dm 2 при напрежение 12 V. Времето за анодиране е 25-30 минути, температурата на електролита не е по-висока от 25 ° C.
2. За необработен дуралуминий плътността на тока е 2-3 A/dm 2 при напрежение 12-20 V. Времето за анодизиране е 20-25 минути, температурата на електролита е около 25°C.
Електролитен метод за копиране на барелефи и декоративни орнаменти
На първо място, от копирания обект или продукт се отстранява отпечатък, тоест се прави калъп от стопяем метал, восък, пластилин или гипс. Копираният предмет, натрит със сапун, се поставя в картонена кутия и се напълва с нискотопима сплав на Ууд или други нискотопими сплави.
След отливането предметът се отстранява и получената форма се обезмаслява и се подлага на медно покритие в електролитна баня. За да не се отлага металът върху тези страни на формата, където няма отпечатък, те се покриват с четка с разтопен восък или парафин.След медно покритие, топимият метал се разтопява във вряща вода и се получава матрица. получени. Матрицата е запълнена с гипс или олово и копието е готово.
За производството на форми се използва следният восъчен състав:
Восък ……………………………… 20 c. з.
Парафин ……………. 3 инча з.
Графит ………………. 1 инч з.
Ако формата е направена от диелектрик (восък, пластилин, парафин, гипс), повърхността му е покрита с електропроводим слой. Проводимият слой може да се нанесе чрез редуциране на някои метали (сребро, мед, никел) или механично чрез втриване в повърхността на люспеста графитна форма с мека четка за коса. Графитът се смила старателно в порцеланов хаван, пресява се през сито или марля и се нанася върху повърхността на продукта с мека четка или памучен тампон. Графитът прилепва по-добре към пластилин. Формите от гипс, дърво, стъкло, пластмаса и папие-маше са покрити с разтвор на восък в бензин. Графитният прах се нанася върху повърхността, която не е имала време да изсъхне, а излишният незалепващ графит се издухва. Поцинкованото покритие лесно се отделя от матрицата с графитно покритие. Ако формата е изработена от метал, тогава върху нейната повърхност е необходимо да се създаде електропроводим филм от оксид, сулфид или друга неразтворима сол, например върху сребро - сребърен хлорид, върху олово - оловен сулфид, така че формата да бъде добре отделен от покритието.
Медните, сребърните и оловните повърхности се обработват с 1% разтвор на натриев сулфид, в резултат на което върху тях се образуват неразтворими сулфиди.
Отлагане на метал върху повърхността на матрицата.Приготвената форма се потапя във вана, чиято верига е захранвана, така че разделителният филм да не се разтваря. Първо, "затягане" (покритие) на проводящия меден слой се извършва при ниска плътност на тока в разтвор от този състав:
Меден сулфат (меден сулфат) ... 150-200 g.
Сярна киселина ……………………………………………………….. 7-15 g
Етанол ………………………………………………………. 30-50 мл
Вода ………………………………………………………… 1000 мл
Работната температура на електролита е 18-25°C, плътността на тока е 1-2 A/dm 2 .
Алкохолът е необходим за увеличаване на овлажняването на повърхността. След като цялата повърхност е „покрита“ със слой мед, матрицата се прехвърля в електролит, предназначен за електроформиране.
За работа с галванично покритие (медно покритие) се препоръчва следният състав:
Меден сулфат (меден сулфат) ...... 340 c. з.
Сярна киселина ………………………………………… 2 c. з.
Вода ……………………………………………………………………. 1000 инча з.
Температурата на електролита е 25-28°C. Плътност на тока 5-8 A/dm 2 .
Методът на метализиране на растения, насекоми и други неметални предмети
За да направите метални листа от растения, с пресни листаотстранете отпечатъците върху восъчната композиция, както следва. Восъчен състав се излива в дебела хартиена форма, оставя се да се охлади до почти пълно втвърдяване, но по такъв начин, че повърхността му да е еластична. След това листата се нанасят върху повърхността на восъка и се притискат със стъкло. Когато стъклото и листата се отстранят, върху восъчната композиция се оставя ясен отпечатък от листата.
След като восъкът се втвърди напълно, матрицата с отпечатъка се графитизира внимателно с мека четка. След като монтират проводниците върху формата, те окачват товара и го спускат галванична вана.
За метално покритие на насекоми (пеперуди, бръмбари и др.), те се приготвят по подходящ начин: насекомите се държат в 1,5% разтвор на сублимат, изсушават се, покриват се с лак или тънък слой восък. След това повърхността трябва да се направи проводима, за това се смазва с четка с течна графитна каша, разредена в алкохол или водка. След изсушаване излишният графит се отстранява.
След това обектът се окачва върху няколко тънки медни жици с диаметър 0,1-0,2 mm, като се усукват или завързват многократно напречно (виж фиг. 4) и се поставят в галванопластична вана.

Ориз. 4.
Висящ бръмбар за медно покритие (а).
Изглед на бръмбар, покрит с метал (б).
За да се елиминира плаваемостта в електролита, пеперуда, буболечка и др. се прикрепя с парафин към стъкло или парче пластмаса. Металът започва да се отлага предимно близо до медните проводници, като се разпространява много бавно към останалата част от повърхността. Следователно в началото на процеса токът трябва да бъде няколко пъти по-малък от нормалното, но когато цялата повърхност е „покрита“ с метал, тя се нормализира. Продължителността на процеса е няколко часа. Дебелината на покритието може да варира от 0,1 до 2 мм.
Използвайки метода на електроформоване, е възможно да се метализира дантела за декоративна и художествена декорация на различни предмети.
Дантелата е опъната върху рамка и импрегнирана с парафин. След това се гладят между листове хартия, за да се отстрани излишният парафин. След това се нанася електропроводим слой от фин графит, излишъкът му внимателно се издухва от дантела. След полагане на проводниците по ръба на дантела те се монтират върху пластмасова рамка или рамка от дебела тел с винилхлоридна изолация, заедно с която дантела се потапя в електролит.
Дантела, покрита с мед, се обработва с месингова четка. Те са запоени с калаено-оловна спойка.
Галваничното завършване на метална дантела се състои в нанасяне на декоративен слой от сребро или злато или в окисляване.
Как да си направим плаки
Методът на изработване на паметни плочи не се различава от метода на изработване на копия от медали, барелефи и др.
Такива дъски обикновено имат текст, рамка, често барелефно изображение (виж фиг. 5).
|
Ориз. 5. Образци на паметни плочи.
Паметна плоча или просто плоча с надпис обикновено се изработва по следния начин. Върху плоска дървена таблетка се изтегля хартия Whatman, чийто размер е малко по-голям от размера на изработената дъска, ръбовете на хартията се залепват към таблета; след това хартията се навлажнява с вода и след изсъхване силно се опъва. На хартия маркирайте местоположението на текста, рамката, барелефа и други детайли, състава на паметната плоча.
Всички детайли от състава на дъската се изработват отделно в съответствие с нейните размери. Барелефът и рамката са изработени по галванопластичен метод и изрязани по контура. Буквите за текста са изрязани от пластмаса, която не се деформира при 60-70 ° C (температурата на излятия восък). Според маркировките на хартията Whatman буквите са залепени върху нея с нитролак. Барелефът предварително се излива от обратната страна с восък за създаване на плоска равнина и също се залепва с нитролак. Монтира се и рамката на дъската. Под барелефа и други части на дъската не трябва да има въздух, тъй като образува черупки по повърхността на восъчната форма.
След това лист хартия Whatman със залепени части се натрива със слънчогледово или рициново масло, така че восъкът да не залепва.
Около така приготвения модел на дъската се монтира черупка под формата на обикновена дървена рамка, чиято височина на стените трябва да надвишава височината на релефа на модела толкова много, че да се получи достатъчно масивна, дебела и се получава трайна форма, която не подлежи на деформация.
Фугата между черупката и дъската се намазва внимателно с глина или пластилин, за да се избегне изтичане на восък.
Приготвеният модел се залива с восъчен композит. След като восъкът се втвърди, черупката се разглобява, восъчната форма се отстранява, обръща се с лицето нагоре и формованите части се отстраняват внимателно от нея. За да премахнете детайли от восъчната форма, особено пластмасови букви, най-добре е да използвате тънко шило или нож с тесен край. След това формата се инспектира, дефектите се елиминират, ръбовете се подрязват.
Подготвената форма се поставя върху пластмасов лист с дебелина 10-15 мм, в който има отвори за фиксиране на формата. След зареждане и нанасяне на електропроводим слой върху формата, той се поставя в вана за покритие.
протозои галванична ваназа електрохимично боядисване на метални части във всякакъв цвят
За електрохимично боядисване на части, изработени от стомана, месинг или мед, е необходимо да се сглобят галванична вана и електрическа верига, както е показано на фигура 6.
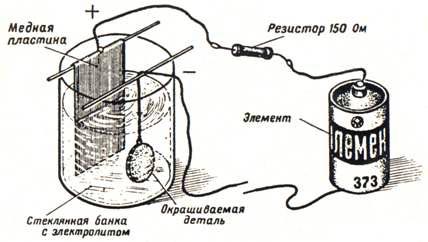
Ориз. 6. Най-простата галванична вана.
Електродът, свързан към положителния извод на елемента, е изработен от листова мед. Минусът на елемента е свързан с частта, която ще бъде боядисана. Трябва да се внимава частите да не докосват медната плоча. В буркана се излива специален електролит и електрическата верига се затваря. След 2-3 минути ще започне оцветяването. Отначало частта ще стане кафява, след това лилава и т.н.
Всичко ще зависи от времето:
2 минути кафяво
3 минути - лилаво,
3-5 минути - синьо,
5-6 минути - синьо,
8-12 минути - жълто,
12-13 минути - портокал,
13-15 минути - червено,
17-21 минути - зелено.
За 1 литър електролит ви трябва:
Меден сулфат - 60 g
Рафинирана захар - 90 g
Сода каустик - 45 g
Пригответе електролита, както следва.Добавете 90 g захар към разтвор на меден сулфат с обем 200-300 ml и разбъркайте добре. Отделно 45 g сода каустик се разтварят в 250 ml вода и към нея се добавя на малки порции разтвор на меден сулфат със захар при непрекъснато разбъркване. След това се добавя вода, за да се получи 1 литър разтвор.
Трябва да се внимава при работа със сода каустик! За да направят цветовете по-контрастни, към готовия електролит се добавят 20 g безводна сол на натриев карбонат. След боядисване детайлът се измива с вода, изсушава се и се покрива с безцветен лак.
Електролитни рецепти за галванични вани
Електролит за бързо медно покритие
Меден сулфат (меден сулфат) - 250 g
Концентрирана сярна киселина - 20 g
Хромен анхидрид - 2 g
Вода - до 1л
Електролит за матово никелиране
Никелов сулфат - 217,5 g
Никелов хлорид - 46,5 g
Борна киселина - 31 g
Вода - до 1л
Работна температура на ваната 50-70°C, плътност на тока 1,5-5 A/dm 2, pH 5,2-5,8.
Електролит за никелиране (твърдо покритие)
Никелов сулфат - 150 гр
Амониев хлорид - 20 g
Борна киселина - 25 g
Вода - до 1л
Работна температура на ваната 50-60°C, плътност на тока 2,5-5 A/dm 2 , pH 5,6-5,9.
Електролит за декоративно хромиране
Хромен анхидрид - 400 g
Концентрирана сярна киселина - 4 g
Вода - до 1л
Електролит за хромиране (твърдо покритие)
Хромен анхидрид - 250 g
Концентрирана сярна киселина - 2,5 g
Вода - до 1л
Работна температура 25-65°C, плътност на тока 20-50 A/dm 2 .
Електролит за калайдисване
Натриев стантанат - 75 g
Сода каустик - 11,5 g
Натриев ацетат - 25 g
Вода - до 1л
Работна температура 65-70°C, плътност на тока 2-4 A/dm 2 .
Електролит за сребро
Сребърен хлорид - 40гр
Желязо-цианоген калий (червена кръвна сол) - 200 g
Поташ - 20 гр
Вода - до 1л
Температура на електролита 20-80°C, плътност на тока 1-1,5 A/dm 2 . Сребърен анод.
Концентрацията на разтвора се характеризира с количеството вещество, разтворено в единица обем вода или друга течност. Концентрацията на разтвора в по-голямата част от случаите трябва да бъде строго определена. Ето защо трябва да се откаже от приготвянето на разтвори на око.
Концентрацията на разтворите се изразява:
1) на части (например 100 части вода, 37 части сярна киселина и 16 части калиев дихромат) или
2) като процент (например 21% воден разтвор на каустик калий).
Понякога концентрацията на разтвора се изразява като съотношение (например, воден разтвор на сярна киселина е 1:10; това означава, че трябва да вземете 1 част сярна киселина и 10 части вода).
Във всички случаи (части и проценти) се имат предвид тегловните съотношения на веществата.
За да определите тегловните количества вода, можете да използвате чаша, като вземете предвид броя кубични сантиметри, съответстващи на броя на грамовете, а за химикали - фармацевтични везни (достатъчна е точност до 0,5 g).
Преизчисляване на водни разтвори от тегловни проценти към части
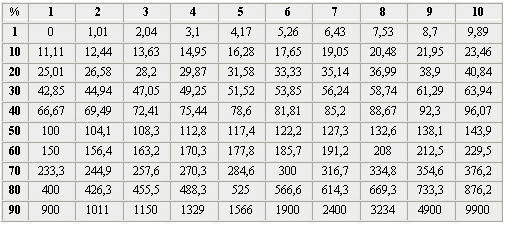
При съставяне на разтвори, чиято концентрация е дадена като процент в таблицата, теглото на разтвора се приема за 100%. Ето защо, например, за да се приготви 21% разтвор на каустик поташ, се измерват 21 части от това вещество и 79 части вода. Такива претегляния не винаги са удобни, тъй като най-често е необходимо да се изхожда от обема или теглото на необходимия разтвор, за да не се приготвя в излишък. След това направете аритметичните преизчисления. Те обаче могат да бъдат избегнати, ако използвате таблицата по-долу, която ви позволява да определите какво тегловно количество вещество е необходимо на 100 части или 100 cm 3 вода, ако процентната концентрация е известна. Например, за 100 cm 3 от 21% воден разтвор на каустик поташ има 26,58 части поташ каустик.
Какво трябва да знаете за химическите несъвместимости
Несъвместимостта на химикалите се проявява във факта, че при случайно смесване, а понякога и при съхранение наблизо, те реагират. Ако реакцията е придружена от отделяне на голямо количество топлина, може да възникне експлозия или спонтанно запалване. В други случаи въздействието на веществата едно върху друго води до тяхното комбиниране и загуба на първоначалните им свойства, в резултат на което веществата стават неизползваеми. Ето някои несъвместими химикали:
Азотната киселина е несъвместима с глицерин, алкохол, етерични масла, смоли, захар, фенол, дървени стърготини, памучна вата.
Алуминиевата стипца е несъвместима с каустични основи (сода каустик, поташ каустик, амоняк), лепило и желатин.
Амонякът (амоняк) и амонякът са несъвместими с формалин (формалдехид) и йод.
Бораксът е несъвместим със стипца, амоняк, сярна киселина, солна киселина.
Йодът е несъвместим с амоняк (амоняк).
Киселините са несъвместими със сапун и алкали (сода, поташ, вар и др.).
Калиевият перманганат е несъвместим с органични вещества - естери, винен алкохол, глицерин, танин, както и с амоняк, амоняк, сяра, йод, въглища.
Сярата е несъвместима с калиев перманганат, белина.
Сярната киселина (витриол) е несъвместима с терпентин, алкохол и бензин.
Алкохолът е несъвместим с хромова киселина, калиев перманганат, лепило, желатин, казеин.
Обезмасляване във вани с разтворители
Силно замърсените части могат да бъдат грубо обезмаслени чрез измиване с керосин или терпентин. След това частите се измиват в технически бензин, технически бензол, ксилен или толуен. Цялостното и окончателно обезмасляване се постига чрез потапяне или изплакване в чист бензин, трихлоретилен или други разтворители.
Недостатъкът на тези вещества е тяхната опасност от пожар и експлозия (бензин, бензол, ксилен, толуол) и токсичността на парите (трихлоретилен, бензин, бензол, ксилен, толуол). Следователно с тях може да се работи само в добре проветриви помещения.
Сега фреоните се използват широко. За разлика от горните вещества, фреонът не е експлозивен, нетоксичен, не разрушава пластмаси, боя и др.
Фреон-113 (трихлортрифлуороетан) е най-добрият обезмасляващ агент от групата на фреоните. Това е силно подвижна прозрачна течност с ниска точка на кипене (47,6°C). Понякога фреон-113 се смесва с други разтворители - ацетон, алкохол и др.
Понякога фреските за обезмасляване са оборудвани с ултразвукови излъчватели или с врящ фреон, което ускорява максимално разтварянето на мазнините. Фреонът не се използва широко поради високата си цена.
Химически разтвор за обезмасляване на цветни метали:
Течно стъкло - 26гр
Тринатриев фосфат - 8 g
Натриев карбонат безводен - 4 g
Вода - до 1л
Всички вещества се разтварят във вода и обемът се довежда до 1 литър.
Отстраняване на метални покрития от продукти чрез електролитен метод (възстановяване)
Възможно е да се отстранят метални покрития от метализирани части и продукти чрез електролитен метод чрез потапяне на частите и продуктите в електролит. Действието на електролита може да се засили чрез свързване на източник на електрически ток към продукта, суспендиран във вана с електролит като анод.
По-долу са дадени няколко рецепти за електролити за отстраняване на метални покрития от части и продукти. Тези вещества се разтварят в 500-600 ml вода и след това обемът на разтвора (електролита) се довежда до 1 литър.
Електролит за отстраняване никелиранеот стоманени изделия
Хромен анхидрид - 240 g
Борна киселина - 30 g
Вода - до 1л
Работната температура на електролита е 85°C, плътността на тока е 1 A/dm 2 .
Електролит за отстраняване на никелови покрития от медни и месингови изделия
Солна киселина - 14 g
Вода - до 1л
Работната температура на електролита е 18-20°C, плътността на тока е не повече от 2 A/dm 2 . Постоянният ток се използва с редовна промяна на полярността. Катодът е въглероден.
Електролит за отстраняване на хромирани покрития от стомана, никел и магнезиеви сплави
Сода каустик - 90 g
Вода - до 1л
Работната температура на електролита е 20°C, плътността на тока е 2 A/dm 2 .
Електролит за отстраняване на калаени покрития от стоманени, медни и месингови изделия
Сода каустик - 120 g
Вода - до 1л
Работната температура на електролита е 18-20°C. Прилага се постоянно напрежение от 6 V с редовна промяна в полярността на източника на ток.
Електролитно полиране на метали
Предметите, които трябва да бъдат полирани, се окачват в електролитна вана като аноди, т.е. към тях се прилага положителен потенциал от източник постоянен ток, токоизправител или батерия.
По-долу са рецептите за полиране.
Електролит за полиране на стомана, желязо и неговите сплави
Сярна киселина концентрирана - 300 мл
Ортофосфорна киселина концентрирана - 600 мл
Вода - 100 мл
Електролитът се приготвя в стъклен или порцеланов съд. Температурата на ваната е около 70°C, плътността на тока е 60-70 A/dm 2 . Полирането продължава 1-5 минути. След изваждането им от ваната, полираните части се измиват в течаща вода, потапят се в 10% разтвор на натриев карбонат и се измиват отново в течаща вода. Изсушете частите на струя топъл въздух.
Електролит за полиране на мед и нейните сплави
Концентрирана сярна киселина - 10 g
Оцетна киселина - 12,5 g
Хромен анхидрид - 12,5 g
Натриев бихромат - 37,5 g
Вода - 1л
Работната температура на електролита е 60-75°C, плътността на тока е 25-50 A/dm 2 .
Полиращ електролит за алуминий
Етилов алкохол денатуриран - 576 мл
Амониев хлорид - 40 g
Цинков хлорид - 180гр
Бутилов алкохол - 64гр
Вода - 128 мл
Полирането се извършва при напрежение 20-14 V. Препоръчително е детайлът да се извади от ваната след 1 минута (това спира пасивирането) и да се потопи отново, като това се повтаря няколко пъти по време на полирането.
Декоративно завършване на изделия от алуминий и неговите сплави
Конструктивните детайли от алуминий и неговите сплави могат да бъдат боядисани във всякакъв цвят.
За тази цел алуминият и неговите сплави се подлагат на анодно окисляване, последвано от адсорбционно оцветяване с различни багрила. Направете го по следния начин. Частите, полирани до огледално покритие, се обезмасляват в разтвор, състоящ се от тринатриев фосфат (50 g), натриев хидроксид (10 g) и течно стъкло (силикатно лепило) (30 g). Изброените химикали се разтварят в 1 литър топла вода в желязна купа (по възможност в тенджера), след което частите за боядисване се поставят за 1-2 минути в този разтвор, загрят до 50-60°C.
Ако тези химикали не могат да бъдат получени, можете да обезмаслите частите с обикновен сапун за пране и топла вода. Детайлите се обработват внимателно с четка с косъм за 10 минути.
Обезмаслените части се измиват със студена вода, след което за отстраняване на оксидния филм се потапят за 2-3 минути в 50% азотна киселина. След това частите отново се измиват обилно със силна струя вода и незабавно се суспендират в анодизираща вана.
Електролитът за анодизиращата вана е разтвор на сярна киселина със специфично тегло 1,12-1,13 при температура 20°C. Когато киселината се смеси с вода, разтворът става много горещ, така че киселината трябва да се добавя към водата на малки порции, като през цялото време разтворът се разбърква със стъклена пръчка.
Ако киселината влезе в контакт с кожата или дрехите, незабавно я измийте със силна струя вода и изплакнете със силен разтвор на сода.
Много добър и по-безопасен е електролит, приготвен от натриев бисулфат (натриева сулфатна киселина), от който 250-300 g се разтварят в 1 л вода. Работната температура на електролита също трябва да бъде не повече от 20°C. Като работна вана можете да използвате емайлирани съдове, керамични, стъклени или пластмасови резервоари.
За анодиране на катоди се използва листово олово, а детайлът служи като анод, който е окачен между два оловни катода на разстояние 70-80 mm от тях. Електролизата продължава 40-50 минути, плътността на постоянния ток е 1-1,5 A/dm 2 . Като източник на ток може да служи батерия с достатъчен капацитет или токоизправител, сглобен на диоди от типа D303 или D305. Трябва да се помни, че само части, изработени от алуминий или неговите сплави, са анодизирани. Закачалки за части се изработват само от алуминий. Всички връзки и контакти трябва да са надеждни, тъй като качеството на анодизирането зависи от това. Заредете части във ваната и ги разтоварете само под ток. След 40-50 минути престой на частите във ваната се разтоварват, измиват се обилно със студена вода и се потапят във воден разтвор на анилиново багрило, загрят до 50-60°С. Разтворът на багрилото трябва да бъде предварително филтриран, тъй като малки зърна неразтворено багрило образуват петна по повърхността на боядисания метал. Цветът на боядисването зависи от времето на престой на анодизираната част в боята, което не трябва да надвишава 15-20 минути.
Анилинови багрила (прахове за боядисване на тъкани) могат да бъдат закупени в магазините за хардуер.
След анодизиране повърхността на чистия алуминий остава лъскава и някои алуминиеви сплавипридобиват матов, тъмен нюанс, който зависи от електрическия режим на анодиране.
За оцветяване се използват 5-10% водни разтвори на следните багрила:
в черно - анилин черен М или анилин прав черен-3;
в кафяво - основно кафяво;
в златисто жълто - директно жълто 2G или ализарин жълто;
в червено - ализарин червен или кисел рубин;
в синьо - киселинно синьо антрахинон или директно синьо М;
в синьо - анилиново синьо или метиленово синьо;
в зелено - директно зелено LC или основно ярко зелено;
в лилаво - основното лилаво.
„Боя оранжево 2G“, „Багрило основно виолетово“ и др. - търговски условия.
Имитация под злато заслужава специално внимание.
Боядисаните части могат да се разграничат от естественото злато само по тегло. Оцветяването е издръжливо и светлоустойчиво. Разтворът за боядисване се приготвя по следния начин. 1 g оранжево багрило 2G се разтваря в 0,5 l гореща вода, към разтвора се добавят 0,1 g жълто-3 багрило и 0,5 g калцинирана сода. След охлаждане разтворът се филтрира. Отделно 0,1 г черно М багрило се разтваря в 0,5 л гореща вода. Този разтвор също се филтрира. Преди боядисване двата разтвора се смесват и се загряват до 50-60°C. В зависимост от времето на престой на частите в това решение можете да получите цвят за всяка проба злато.
Възможно е боядисване на анодизирани части от алуминий и неговите сплави не само в посочените разтвори на органични багрила. За целта можете да използвате и изброените по-долу цветни неорганични съединения, които се образуват директно в порите на анодизирания метал след последователно потапяне първо във воден разтвор "а", след това във воден разтвор "б".
Например за оцветяване в бялосе използват разтвори:
а) оловен ацетат, 10% разтвор,
б) натриев сулфат (Глауберова сол), 10% разтвор;
в синьо или светло синьо:
а) калиев ферицианид, 50% разтвор,
б) железен хлорид, 5-10% разтвор;
до златисто жълто
а) хипосулфит, 5% разтвор,
б) оловен ацетат, 5% разтвор;
до портокал:
а) калиев хромат, 2-3% разтвор,
б) сребърен нитрат, 5-10% разтвор;
до жълто:
а) калиев дихромат, 2-5% разтвор,
б) оловен ацетат, 10-15% разтвор;
до кафяво:
а) калиев ферицианид, 2-5% разтвор,
б) меден сулфат, 5-10% разтвор.
След адсорбционно оцветяване частите се измиват с гореща вода и се потапят за 2-3 минути в разтопен восък или парафин, след което, докато са още горещи, се избърсват с марля.
Най-простата инсталация за галванично покритие на метални повърхности
В ремонтната и любителската практика може успешно да се използва миниатюрна безвана галванична инсталация (виж фиг. 7).
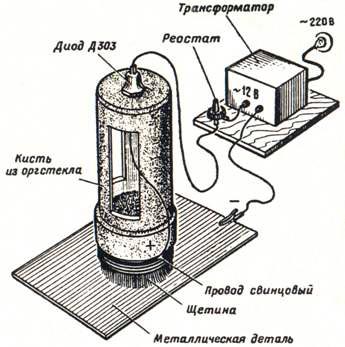
Ориз. 7. Миниатюрна галванична инсталация.
Състои се от специална четка с влакна (диаметър на четката 20-25 мм, тялото й е направено от органично стъкло с дебелина 5-6 мм, вътре в което се излива електролит), понижаващ трансформатор за напрежение 12 V и ток от 0,8-1 A или батерия и свързващ кабел. Влакната на четката са обвити с оловна (в краен случай, калайдисана медна) тел. Върху тялото на четката е монтиран полупроводников диод от тип D303-D305. Единият от проводниците на понижаващата намотка на трансформатора е свързан към анода на диода, а другият, с помощта на щипка тип алигатор, към частта, която трябва да бъде покрита. Катодът на диода е свързан към проводника за навиване на четката. Ако се използва батерия, диодът не е необходим.
Частите, които ще бъдат покрити, се почистват от ръжда, мръсотия и мазнини, избърсват се със суха чиста кърпа и се обезмасляват в разтвор, съдържащ 100-150 g сода каустик, 40-50 g калцинирана сода и 3-5 g течно стъкло ( силикатно лепило) на 1 литър. В зависимост от степента на замърсяване частите се държат в обезмасляващ състав, загрят до 80-100 ° C, от 15 минути до 1 час. Колкото по-гладка и по-чиста е повърхността, толкова по-здраво ще бъде поцинкованото покритие. Подготвената част е свързана към намотката на трансформатора, електролитът се излива в четката и захранването се включва. Равномерно движете четката по повърхността на детайла, покрийте я с метал, отложен от електролита. За да се получи покритие с достатъчна дебелина, е необходимо да се премине с четка един по един и едно и също място 20-25 пъти. Електролитът се добавя към четката, когато се изразходва. След намазването детайлът се измива в течаща вода и се полира във влажна вода с кърпа, след което се измива отново и се суши.
За всеки тип покритие се приготвя специален електролит според следните рецепти(в грамове на 1 литър разтвор):
Електролит за медно покритие
Меден витриол (меден сулфат) - 200
сярна киселина - 50
Етилов алкохол или фенол - 1-2
електролит за никелиране
Никелов сулфат - 70
Натриев сулфат - 40
Борна киселина - 20
натриев хлорид - 5
Електролит за хромиране
Хромен анхидрид - 250
Сярна киселина (sp. w. 1,84) - 2,5
Електролит за поцинковане
Цинков сулфат - 300
Натриев сулфат - 70
Алуминиева стипца - 30
Борна киселина - 20
Електролит за сребро
Прясно утаен сребърен хлорид - 3-15
Желязо-цианоген калий - 6-30
Електролит за позлатяване
Хлорно злато - 2,65
Желязо-цианоген калий - 15-50
Калцинирана сода - 20-25
В 200-300 ml дестилирана вода се разтваря по ред първото вещество, след това второто, третото и т.н., след което се добавя вода към 1 литър.
Трябва да се има предвид, че въпреки че разтворите не съдържат силно токсични вещества, с тях трябва да се работи внимателно, за да се избегнат изгаряния и отравяния. Разтворите се съхраняват най-добре в тъмен стъклен съд със смляна запушалка.
Също така трябва да се има предвид, че не всички покрития пасват добре на различни метали. Например, за да се покрие стоманена част с никел, тя е предварително покрита с тънък слой мед, докато хромът прилепва добре към никелирана повърхност. Преди никелиране или сребърно покритие е желателно да се нанесе меден подслой върху части, изработени от бронз. Медните и месинговите части са посребрени без меден подслой.
Статията е съставена според публикациите на V.G. Бастанов
Автор-компилатор.Патлах В.В. 1996 г
© "Енциклопедия на технологиите и методите" Patlakh V.V. 1993-2007 г
Галванопластика у дома
Създаване галванични покрития вкъщи
Галваничните декоративно-защитни или технологични покрития върху метални изделия са тънък повърхностен слой от друг метал, който има по-добри технологични или антикорозионни свойства и добър естетичен вид (например никел, хром, сребро, цинк). Когато се подготвя за извършване на галванична работа, любителският майстор трябва да разполага с мощно заземено DC захранване с непрекъснато регулируема изходна мощност с максимален ток 20 A. Това може да бъде фабрично произведен токоизправител или прост, но мощен самостоятелно изработен токоизправител.
Едно от най-важните условия за получаване на висококачествено галванично покритие е предварителната подготовка за пясъкоструене, шлайфане, обезмасляване и продукти.
Смилането се извършва механично с помощта на четка, шлифовъчни пасти и шмиргели.
Обезмасляването на подготвените части се извършва в органични разтворители: алкохол, бензин, ацетон, бензол, трихлоретилен. Подготвяната част се измива старателно в разтворители, като се обръща внимание на труднодостъпните места, до които е трудно да се приближи. Индикатор за висококачествено обезмасляване е доброто намокряне на повърхността на детайла с вода. Продуктите от чугун и стомана се обезмасляват много добре, като се използват следните разтвори:
Сода каустик....................... 10-20 г калцинирана сода... 50 г Течно стъкло............. ... 5-15 гр. Вода...................... 1000 гр
Сода каустик.............................50 g Кацинирана сода......30 g Натриев фосфат..... .. 30 g Течно стъкло................................5 g Вода............. ........................ 1000 гр
Температурата на разтворите по време на обработката на детайла трябва да бъде 60 ÷ 90 градуса. C. Работата трябва да се извършва в защитни ръкавици и престилка, не позволявайте капки от разтвора да попаднат върху кожата и очите.
За продукти от цветни метали съществуват следните решения:
Натриев фосфат ...... 10-20 g Сапун за пране ...... 10-20 g Вода ................... ..... 1000 гр
Сода каустик .................................10 g Натриев фосфат....... 50-60 Вода.. .................................................... 1000 гр
Работна температура на първия разтвор - 90 градуса. С, а вторият - 60 градуса. ОТ.
обезглавяване- процесът на отстраняване на оксидния филм от повърхността на метална част преди галванична обработка. В домашната работилница можете да използвате следните разтвори за мариноване:
концентриран сярна киселина.... 70-80 Хромиран връх ........................................ ...... ... 2-3 Вода ................................ .......... сто
Солна или сярна киселина .......... 5 Вода .......... 100
Броят на компонентите е посочен в масови части. Времето за обработка на детайлите с първото решение е 20 s, а с второто - 60 s.
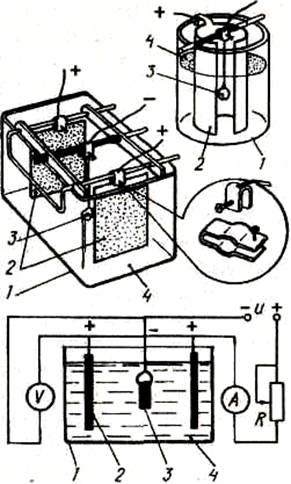
Ориз. : Схема и оборудване за галванопластика 1 - контейнер, изработен от химически неутрален материал, като стъкло; 2- аноди; 3- детайл (катод); 4- електролит
Сега помислете за технологията за създаване на галванични покрития.
никелиранеизползва се за получаване на декоративни покрития и за образуване на междинни слоеве в многослойни покрития (например при хромиране). Никеловите покрития имат красив външен вид, устойчивост на атмосферни влияния, не създават трудности при нанасяне метални части.
Оборудване за никелиране(както и за всички останали покрития) е показано на фигурите.
Никелиран в слабо кисел електролит, със следния състав:
Никелов сулфат 140 g Натриев сулфат 50 g Магнезиев сулфат 30 g Натриев хлорид (чиста готварска сол) 5 g Борна киселина 20 g Вода 1000 g
Температурата на електролита е 18÷25ºС, плътността на тока е 0,8÷1,2 A/dm2.
Ако нямате магнезиев сулфат и натрий, количеството никелов сулфат в електролита се увеличава до 250 g, натриев хлорид - до 25 g, борна киселина - до 30 g, докато никелирането трябва да се извършва на електролит температура 50 ÷ 60ºС и плътност на тока 3 ÷ 5 A /dm2.
Химикалите, включени в електролита, се разтварят във вода отделно, разтворите се филтрират старателно, след което се смесват. Качеството на покритието зависи от киселинността на електролита (рН). За нашия случай - pH 4÷5. При тази киселинност лакмусовата хартия става червена. Ако киселинността на електролита е по-висока, към него се добавя воден разтвор на амоняк в малки количества. Неизправностите в никелирането причиняват намаляване на плътността на тока, което води до образуване на сив налеп и увеличаване на плътността на тока, до появата на крехък нехомогенен никелов слой. При използване на електролит с pH по-високо от b, върху покритието се появяват бели петна, а по-малко от 4 - покритието е хетерогенно. Слой от никел с дебелина 1 μm при плътност на тока 0,15 A/dm2 се утаява за 20 минути, а при 0,1 A/dm2 за 30 минути.
След приключване на процеса на никелиране, продуктът се измива във вода, изсушава се и внимателно се полира върху филцово колело с помощта на полиращи пасти.
Хромирането на метални части се използва за повишаване на твърдостта (функционалността) и устойчивостта на корозия, получаване на отразяващи повърхности и декоративен ефект. Искам да отбележа, че хромовите покрития са порести, следователно под тях, на повърхността на черни метали, трябва да се използва междинен слой от мед или никел, ако това се пренебрегне, под слоя хром ще възникнат корозионни процеси. За да се избегне това, се използват многослойни галванични покрития, например мед-никел-хром или никел-мед-никел-хром. Качеството на хромовите покрития зависи от концентрацията на електролита, плътността на тока и температурата на електролита. Чрез регулиране на температурата на електролита е възможно да се получат различни нюанси на покритията: при температура 35÷55ºС покритието е лъскаво; при 55÷80ºС - млечни; при температури под 35ºС - тъп.
Що се отнася до анодите, които, както показва практиката, осигуряват най-стабилните процеси на хромиране, можем да препоръчаме производството им от следната сплав: олово - 81 ÷ 86%, калай - 10 ÷ 15%, антимон - 4%. Въпреки това, не винаги е възможно да се намерят такива аноди, като в този случай можете да използвате изцяло оловни аноди или аноди от сплав от 93% олово и 7% антимон.
В зависимост от състава на електролита е възможно да се получи доста широка гама от покрития, различни по цвят и физически параметри.
Декоративното хромово покритие се получава чрез използване на електролит от следния състав, от който се състои електролитът; 350 масови части (m.h.) хромен анхидрид, 3.5 m.h. сярна киселина и 100 м.ч. вода. Температурата на електролита по време на хромиране трябва да бъде 35 ÷ 40 градуса. C, а плътността на тока е 10÷15 A/dm2.
Устойчивото на износване хромирано покритие се използва за обработка на части на двигатели, скоростни кутии, хидравлика и други механизми. Получава се с помощта на електролит със следния състав: 150 m.h. хромен анхидрид, 1,5 m.h. сярна киселина и 100 м.ч. вода. Температура на електролита 50÷55ºС, плътност на тока 45÷100 A/dm2.
Получава се тъмносиньо декоративно и защитно покритие с електролит със следния състав: 350 m.h. хромен анхидрид, 3,5 m.h. сярна киселина, 1 m.h. жълта кръвна сол и 100 м.ч. вода. Температура на електролита 25÷30ºС, плътност на тока 5÷10 A/dm2.
Ахатово, тъмносиньо декоративно и защитно покритие се получава чрез използване на електролит, състоящ се от 40 m.h. хромен анхидрид, 10 m.h. бариев ацетат и 100 m.h. вода. Температурният режим на електролита е 15ºС, плътността на тока е 25 A/dm2.
Черно декоративно и защитно покритие се получава, ако се използва електролит със следния състав: 250 m.h. хромен анхидрид, 8 m.h. калциев ацетат и 100 m.h. вода. Температурният режим на електролита е 25÷30ºС, плътността на тока е до 100 A/dm2.
Меко декоративно покритие се получава чрез обработка в електролит със следния състав: състоящ се от 250 m.h. хромен анхидрид, 7÷10 m.h. хромов сулфат, 3 m.h. борна флуороводородна киселина, 100 m.h. вода обаче може да се използва и друг състав: 250 м.ч. хромен анхидрид, 3,5 m.h. натриев флуорид и 100 m.h. вода. И за двата електролита плътността на тока е 4÷5 A/dm2, а температурата е 18÷20ºС.
Електролитите не могат да се съхраняват дълго време, защото се губят първоначалните им качества.
Продуктите от чугун и стомана се нагряват до работната температура на електролита преди обработка, медните и месинговите продукти се загряват предварително в гореща вода и след това се потапят в галванична баня под напрежение.
Алуминият и неговите сплави са покрити със здрав филм от друг метал преди хромиране. За да направите това, трябва да потопите продукта, чиято повърхност е подготвена за хромиране, в разтвор от следния състав: железен хлорид - 25 ÷ 35 g, концентрирана солна киселина - 15 ÷ 20 g, вода - 1000 g Частта се държи в този разтвор за 1 ÷ 2 минути, след това се измива с вода и веднага се пристъпва към хромиране. Можете да използвате и друг разтвор: цинков сулфат - 200 г, сода каустик - 200 г, вода - 1000 г. В този разтвор алуминиевата част трябва да се държи 2 ÷ 3 минути, след което да се изплакне с вода. В този случай върху повърхността на продукта се образува тънък междинен слой цинк, който ще осигури добра адхезия на хромираното покритие към детайла.
Понякога трябва да актуализирате хромираното покритие на продукта. За да направите това, продуктът трябва да бъде потопен в електролита и за 30 s трябва да се пропусне обратният ток. В същото време повърхността на старото хромирано покритие е леко разтворена и бъдещото хромирано покритие надеждно прилепва към старото. При нанасяне на хромови покрития плътността на тока се настройва до изчислената стойност за 3÷5 min.
След приключване на галваничния процес продуктът се отстранява от електролита, измива се в топла вода, след което се неутрализира в 3% разтвор на сода бикарбонат, след което се измива отново в гореща вода и се суши. Ако се нанесе твърдо устойчиво на износване покритие, продуктът трябва да се вари 1 ÷ 1,5 часа в голям обем дестилирана вода, накрая се поставя за 2 ÷ 4 часа във фурна с температура 110 ÷ 130ºС .
В края на хромирането механичното полиране задължително се извършва с помощта на полиращи пасти.
Поцинковане, като правило, се използва за създаване на защитни антикорозионни или декоративни покрития върху повърхността на черни метали. Цинкът силно прилепва към повърхността на други метали и с течение на времето върху цинковите покрития се образува тънък филм от оксиди, който има добри защитни свойства. За галванично поцинковане се използва електролит със следния състав: цинков сулфат - 200 g, амониев сулфат - 50 g, натриев ацетат - 15 g, вода - 1000 g.
ЦинкиранеПоцинковането е широко разпространено. За цинкиране се използва електролит със следния състав: цинков оксид - 4 ÷ 5 g, каустик поташ - 85 ÷ 100 g, калаен хлорид или калаен хлорид - 0,15 ÷ 0,25 g, водороден прекис - 2 t, вода - 10 g. Работна температура на електролита - 50ºС, плътност на тока - 0,5 A/dm2.
Електролити за поцинкованесе приготвят в следната последователност: първо, каустичният поташ се разтваря във вода, като се използва 1/10 от обема на цялата вода, разтворът се нагрява до температура 90 ÷ 100ºС и в него се разтваря цинков оксид. Разтворът се разрежда с гореща вода до половината от обема на ваната и се разбърква добре. Цинковата сол, която се образува в този случай, се защитава дълго време и след това внимателно се излива в работната баня. Хлоридът или хлорният калай се разтварят във вода отделно и се изсипват в електролита още в процеса на галванична обработка.
След обработка може да се даде блясък на поцинкован продукт за декоративни цели. За да направите това, продуктът се спуска за 2 ÷ 3 s в разтвор от следния състав: хромпик - 100 ÷ 150 g, сярна киселина - 3 ÷ 4 g, вода - 1000 g. Можете също да използвате 2 ÷ 3% разтвор на азотна киселина за тези цели. След обработка продуктът се измива обилно с вода.
Медно покритие на метални частипроизвежда се за защитни цели и преди хромиране, както и за създаване на проводящ слой върху металната повърхност с минимално съпротивление. За висококачествено покритие на черни метали със слой мед се използват цианидни електролити, с които е неприемливо да се работи у дома. Следователно стоманените и чугунените части първо се никелират и едва след това върху никела се отлага мед. При медно покритие на никелирани продукти можете да използвате електролит със следния състав: меден сулфат (меден сулфат) - 200 g, концентрирана сярна киселина - 30-50 g, вода - 1000 g. Работната температура на електролита е 18-25ºС, плътност на тока - 1-2 A / dm2.
При покриване на алуминиеви продукти със слой мед, също така е необходимо да се извърши предварителна подготовка. След мариноване алуминиевият продукт се окислява за 10-15 минути в електролит със следния състав: концентрирана сярна киселина - 109 g, вода - 1000 g, при температура 18-25ºС и плътност на тока 1 A/dm2. След това продуктът се ецва във воден разтвор на сода (30 g на 1000 g вода) за 3-4 минути при температура 50-55ºС. След ецване детайлът се измива обилно с вода и се потапя в галванична баня с електролит със следния състав: меден сулфат - 188 g, сярна киселина - 49 g, вода - 1000 g. Работната температура на електролита е 15-20ºС, плътността на тока е 1 A / dm2. Като анод се използва медна плоча.
Месингово покритиее нещо междинно между медно покритие и поцинковане. За електролита се използват реагенти, използвани както за медно покритие, така и за поцинковане: меден сулфат (меден сулфат) - 5 g, цинков сулфат - 8,5 g, оксалова киселина - 30 g, концентрирана киселина - 20 g, желатин - 0,2 g, вода - 1000 гр. Работна температура на електролита - 18-25 градуса. C, плътност на тока - 2-3 A/dm2.
Посребряване с галванично покритиеИзползва се за създаване на декоративни защитни и електропроводими слоеве върху повърхността на металите. Сребърните продукти също имат добра отразяваща способност. При посребряване на части от черни метали първоначално се създава междинен слой от никел чрез галванично никелиране, върху който се отлага сребро. Електролитът за галванично сребро се състои от следните компоненти: сребърен хлорид - 10-15 г, жълта кръвна сол (калиев железен цианид) - 15-35 г, калцинирана сода - 15-35 г, вода (за предпочитане дестилирана) - 1000 г. Електролит работна температура - 18-20град. C, плътност на тока - 0,1 A/dm2. Като анод се използват графитни плочи. Всеки компонент на електролита се разтваря отделно във вряща вода. Сребърният хлорид се разтваря на тъмно място. Разтворите на жълта кръвна сол и калцинирана сода се изсипват в разтвор на сребърен хлорид и се варят заедно 1,5-2 часа, след което всичко се филтрира. Готовият електролит има светложълт оттенък и не включва утайка.
Нанасянето на галванични покрития чрез триене ви позволява да правите без галванични процеси, това е особено ценно при обработка на големи части. За да приложи този метод, аматьорски майстор трябва да направи малко устройство. Необходимо е да има понижаващ трансформатор с
 Ориз. Устройство за галванично покритие чрез триене
Ориз. Устройство за галванично покритие чрез триене
изходно напрежение 5-15 V (за предпочитане непрекъснато регулируемо) и ток до 2 A, диоден мост (могат да се използват диоди DZOZ-D305), четка с диаметър 20-30 mm, свързващи проводници. Четката за галванично покритие е универсален инструмент за създаване на галванични покрития от всякакъв метал. Дръжката на галванична четка е направена от диелектрични материали. Можете да използвате парче пластмасова тръба с подходящ диаметър. Отгоре дръжката трябва да бъде плътно затворена с пластмасов капак, а отдолу - с вложка, изработена от четина или каквато и да е синтетична купчина. Вложката трябва да се опира в дъното на летвата, което е на 20 мм над долния разрез на пластмасовата тръба. Настръхната вложка е силно обвита с метална тел, за да изглежда като дебела четка. Този проводник действа като анод. Тел от неръждаема стомана се използва за поцинковане, хромиране, никелиране, сребърно покритие и позлата, но при никелиране под него се поставя извита никелова плоча, а при хромиране се използва олово. При медно покритие се използва обикновена медна тел. В домашната работилница е необходимо да имате няколко вложки от четина с различен диаметър, които се използват за покриване с различни метали. Проводникът на вложката е свързан чрез свързване на проводници към положителния контакт на захранването. Сноп четина с диаметър един и половина до два пъти по-голям от диаметъра на пластмасова дръжка се завързва с найлонов конец. Върху него се навива подходяща тел, докато се образува колан, върху който ще се опира тръбната дръжка. Между дръжката и пояса се полага гумено уплътнение под формата на лента с дебелина 1-1,5 мм и с подходяща дължина. Когато правите вложката, можете да използвате влакната на четката за боядисване. Ако космите в четката са свързани с епоксидно лепило в основата, тогава тази част ще трябва да бъде отрязана, тъй като слоят от лепило ще предотврати проникването на електролита в работната зона. Дължината на четината трябва да бъде 45-60 мм, от които 20 мм ще влязат в дръжката, 10 мм ще се скрият под намотката на жицата, 15-20 мм ще съставляват свободния край. Ако е необходимо, краят на четката се шлайфа върху шмиргел до получаване на равна повърхност. За да работи, електролитът се излива в дръжката, вложката е свързана към положителния извод +, а детайлът е свързан към отрицателния извод на източника на захранване--. Инструментът се движи равномерно по повърхността на продукта, без да се откъсва от него. Периодично към писалката се добавя електролит (не се допуска пълно изпразване на писалката). За да се получи добро покритие върху определена площ от повърхността на продукта, е необходимо да се направят 15-30 прохода на галваничната четка. Можете да използвате и по-лесно за направа устройство. За да направите това, плоча от мед, олово, цинк, никел или неръждаема стомана, в зависимост от вида на необходимото покритие, се свързва с проводник към положителния извод на източника на захранване, след което се увива с фланелен плат със слой от 4 -5 мм, фланелата се навлажнява с електролит и се разтрива, обезмаслява и обезглавява обект, към който е свързан отрицателният извод на източник на захранване. Плочата във фланелата трябва да се навлажнява много по-често в електролита. Необходимо е да се работи в очила и в защитни гумени ръкавици. Електролитите за галванично покритие чрез триене могат да бъдат същите като при класическото галванично покритие, но все пак е по-добре да използвате следните състави:
медно покритиеМеден сулфат...............200 g Концентрирана сярна киселина.................50 g Етилов алкохол или фенол..... ........1-2 g Вода ........................1000 g
Хромирано покритиеХромен анхидрид .........250 g Концентрирана сярна киселина .................. 2,5 g Вода ............. ........................................ 1000 гр
никелиранеНикелов сулфат......70 g Натриев сулфат......40 g Борна киселина................20 g Натриев хлорид...... .. ...5 g Вода ................................. 1000g
ПоцинкованеЦинков сулфат .......... 300 g Натриев сулфат ..... 70 g Борна киселина .................. 20 g Вода .... .................................... 1000 гр
ПосребряванеСребърен хлорид (прясно утаен) .......... 10-15 g Жълта кръвна сол ......................... .................... 15-30 г калцинирана сода ......... ........................ 15-30 г вода ........................ ........................................................ ... 1000 g След нанасяне на покритието продуктът се измива обилно с вода, изсушава се и се полира с полиращи пасти.
Методи за галванично покритие
Всичко галванични процесипродължете по доста прост модел. Има система, състояща се от продукт, върху който се нанася някакво покритие, разтвор, в който се поставя този продукт ( електролит). И третият компонент е плочата, към която се прилага положителен заряд и се нарича анод. Продуктът от своя страна действа като катод и върху него се прилага отрицателен заряд. Когато такава система е свързана към източник на захранване, металът, от който се състои анодът, се разтваря в електролита и металът, разтворен в електролита, се прилага върху продукта. Електролитът действа като метален носител от анода към нашия продукт. Размерите на ваните, където се излива електролитът, могат да бъдат много различни, от фракции от литър до десетки тонове. Самите размери и форма на ваните са продиктувани от размерите на продуктите, които са предназначени да покриват. Баните са покрити с продукти, които могат да бъдат окачени на висулки. Чрез тях към продукта ще се подава минус от източника на захранване и те ще задържат продукта на тегло в обема на електролита.
Ако продуктите са много малки и има много, прибягват до помощта на леко модифицирани вани, които се наричат барабани. В барабаните се покриват няколко продукта наведнъж и контактът с минуса на източника на енергия се осигурява поради техния взаимен контакт. В барабаните продуктите също се търкалят едновременно с покритието. Самият барабан с продуктите се върти в електролитна вана, която съдържа и анода.
По подобен начин са подредени вани от насипен тип. В тях също се изсипват продукти, излива се електролит и там се вкарва анод. Те се въртят бавно и частите, преливащи се в електролита, бавно натрупват покритието.
И трите от тези метода осигуряват пълно покритие на продуктите от всички страни. Но има и друг метод на галванопластика и той се нарича трибогальванопластика, стилоелектропластика, триене и т.н. Значението му е, че както обикновено, минусът на източника на енергия се подава към продукта, плюс към анода, но цялата тази система не е потопена в електролита. Електролитът се импрегнира само с парцал или тампон, навит около анода. Анодът, който се държи в ръката под напрежение, като че ли разтрива продукта и след известно време върху продукта се появява покритие. Електролитите за този метод на приложение често се наричат гелове. Това са просто сгъстени електролити, така че да се оттичат по-малко от тампона върху продукта. С този метод е възможно да се покриват големи продукти за много дълго време, но не целият продукт, а само до необходимите повърхности. Недостатъкът на този метод е силното изменение в дебелината на нанесеното покритие и като правило се оказва много тънко. Такова покритие е рязко по-ниско по качество от покритията, нанесени във вани, държи по-лошо и не е еднакво на цвят.
Отделни, но много близки до галваничните, са методите за химическо и потапящо отлагане на метални покрития. В електролитите, за да настъпи редукция на метални атоми на повърхността на продукта, е необходим поток от електрически ток. По време на химическото отлагане се създава система, в която се въвежда редуциращ агент. Той е този, който, окислявайки, възстановява покритието на метала върху повърхността на продукта. Това е така наречената автокаталитична реакция, която протича само на повърхността на металния катализатор. И катализаторът е същият метал, който се прилага. Накратко това се случва по следния начин: приготвя се разтвор (понякога се нагрява), приготвеният активиран продукт се спуска там и се извършва нанасянето. Не винаги обаче е лесно да се започне такава реакция, понякога тя започва сама от по-активни метали, а понякога трябва да се стартира принудително, с помощта на катализатор, например паладиеви наночастици. И тук е най-важното! По този начин е възможно да се покриват не само метални части, изработени от различни сплави, но и непроводими материали, като пластмаси. Методът на потапяне, за разлика от химическия, протича под формата на обменна реакция на повърхността на метален продукт. Решение за например потапящо позлатяване гравира метала върху повърхността на артикула и вместо това отлага злато. Това е просто реакция на размяна. Продължава, докато на повърхността остане само злато и няма повече гол, различен неблагороден метал.
Точно на химични процесиотлагането на метал се основава на технологията за метализиране на непроводници, пластмаси, тъкани и др. Според тази реакция се създава проводящ слой и вече върху него с обикновен галванични методивсички останали покрития се нанасят, включително финишното покритие.
Всички други методи за нанасяне на метални покрития, като вакуумно и плазмено пръскане, не са галванични методи.
Нанасянето на слой цинк върху желязото е най-разпространеният начин да го предпазите от корозия. Галваничното поцинковане е най-разпространено поради предимствата на технологията и получените защитни покрития.
1 Характеристики на защитните цинкови покрития
Поцинковането е най-разпространеният начин за защита на желязото от метализиране на повърхността. За тези цели се изразходва около 40% от общото световно годишно производство на цинк. Поцинковането стана широко разпространено поради анодния характер на защитата, създадена от цинк.
Стойността на електрохимичния потенциал на цинка е - 0,763 V, което е по-малко от същия параметър за черни метали (желязо, стомана, чугун), така че предпазва последните от корозия електрохимичен начин. Освен това защитните свойства на цинковите покрития се проявяват дори в случай на тяхната незначителна дебелина и при наличие на открити зони, пори. Има много примери за защитната природа на цинковата защита на непокрити, оголени фрагменти от стоманени продукти (например отрязана тел в напречно сечениеи ръбове, резба на гайка без покритие, завинтена върху поцинкован болт).
Анодният характер на взаимодействието на цинковото покритие със стоманата и околната среда в някои случаи може да се промени в катоден, а след това корозионните процеси в желязото протичат много интензивно. Това се наблюдава, например, когато гореща вода, загрята до 70 ° C и повече, е изложена на поцинковани продукти (в автоклави, котелни инсталации).
Самият цинк, поемащ "удар" от външната среда, е защитен по следния начин: когато този метал се окисли, върху повърхността му се образува тънък плътен оксиден филм, който предотвратява проникването на кислород по-нататък в цинка. Поради това окисляването му спира. В желязото образуваните по време на окисляването оксиди имат обем, по-голям от първоначалния метал, и следователно филмът от тях незабавно се срутва, става рохкав и предава кислород към неокисления материал. Така възниква ръждата.
За цинкови покрития химическата устойчивост се намалява, когато са изложени на летливи продукти, които се отделят по време на стареене на следните органични материали:
- изсушаващи масла;
- синтетични смоли;
- хлорирани въглеводороди.
Покритията са подложени на лесно разграждане, ако влязат в контакт или са в затворен обем с намаслени или прясно боядисани части.

pH на средата има голямо влияние върху скоростта на корозията на цинка. При pH 7–12 (алкално) този метал практически не се разтваря. Отклонението от тези стойности води до увеличаване на скоростта на неговата корозия. Скоростта на корозия на цинковите покрития е особено висока в атмосферата на тропиците и индустриалните градове.
2 Галваничен метод на поцинковане на метали
Защитният ефект на цинковите покрития се определя преди всичко от тяхната дебелина, която се определя въз основа на специфичните условия на работа. метални изделияи тяхната еднородност.Възможностите на различните методи на поцинковане не са еднакви и позволяват получаване на покритие от 5 микрона (поцинковано) до 1,5 мм. Кога метод на галванично покритиеметализация, качеството на защитния слой до голяма степен зависи от естеството на електролита, използван за поцинковане.

Защитните свойства на цинка могат да бъдат значително увеличени по различни начини, най-често срещаните от които са както следва:
- пасивиране (хромиране) - създаване на хроматни филми върху повърхността му чрез химическа обработка на продукти в разтвори с хромова киселина или нейни соли;
- фосфатиране - образуването на фосфатен филм върху повърхността му чрез обработка на поцинковани заготовки в разтвори на соли на фосфорната киселина;
- боядисване - нанасяне на бояджийски покрития (най-добри резултати след предварително фосфатиране).
Галваничното поцинковане е електролитен метод за нанасяне на тънък защитен слой цинк върху продукт, чиято повърхност трябва да бъде предварително подготвена. Този метод дава възможност да се получат покрития с дебелина 5-40 µm.

При условията на мащаб, лист, лента дебелината може да се увеличи до 500 микрона (0,5 мм). Самият процес на образуване на покритието се състои в отлагането върху катода (продукта, който е покрит) на положително заредени частици (йони) на цинк от водни разтвори на неговите съединения (електролити), когато през разтвора се пропуска постоянен електрически ток. Използваните аноди трябва да бъдат изработени от цинк, тъй като основната им цел е да попълват йоните, отделяни върху продуктите в електролита. В зависимост от избрания режим, токът има катодна плътност в диапазона от 1–5 A/dm 2 .
3 Предимства и недостатъци на цинковото покритие
Електролитният метод за нанасяне на цинк, в сравнение с други методи за поцинковане, е най-разпространеният и има следните предимства:
- висока производителност;
- ниска цена;
- получаване на достатъчно високо ниво на защита на продукта;
- равномерно покритие без ивици, капки, като същевременно се запазва формата и размера на продукта;
- възможността за нанасяне на цинк върху всички части на продукти с всякакви сложна форма, включително различни пори;
- получаване на декоративни защитни покрития (гладки, лъскави), които не изискват допълнителна обработка.

Основният недостатък е ниската адхезия (адхезия) на образуваното покритие с продукта, което изисква специални грижи при подготовката (почистването) на повърхността на последния. Трябва също да се отбележи, че има вероятност защитеният метал да бъде хидрогениран, особено ако не се спазват режимите на цинково поцинковане, което води до водородна чупливост на продукта и непривлекателен външен вид на повърхността му. Съществен недостатък на този метод е образуването на токсични и вредни за околната среда отпадъци, които трябва да бъдат подложени на цялостно почистване.

4 Технология и оборудване за поцинковане в производството
При производството електролитното поцинковане включва следното технологични процесипроизведени с продукти:
- Почистването им от котлен камък, ръжда, смазочно-охлаждащи и бояджийски и лакови състави. Химическа обработка в обезмасляващи и алкални разтвори.
- Измиване с вода в течаща баня.
- Електролитно обезмасляване.
- Зачервяване.
- Гравиране в разтвор на вода и солна киселина. Позволява отстраняване на остатъчния котлен камък и ръжда без разтваряне на основния метал. В този случай повърхността се обезглавява - активиране преди поцинковане.
- Зачервяване.
- Просто поцинкована.
- Зачервяване.
- Избистрянето може да се извърши в разтвор на вода с азотна киселина за отстраняване на оксидния филм.
- Зачервяване.
- Може да се извърши фосфатиране.
- Зачервяване.
- Може да се извърши пасивиране чрез електролитно хромиране (и/или спрей хромиране).
- Изсушаване.

В зависимост от вида на продукта и използваната технология, някои от стъпките на пране могат да се извършат с помощта на метода на измиване с четка. Възможно е да има допълнителни операции. Например, галваничното поцинковане на лента започва с нейното развиване, заваряване на краищата и след това изправяне. Финиш - смазване и навиване.
В съответствие с вида на продуктите, които се покриват, и обема на производството се използват различни линии за поцинковане и свързаното с тях оборудване. допълнително оборудване. Тези линии представляват определена последователност от миещи и технологични бани, необходими за създаването на еднослойни или многослойни цинкови покрития с необходимите функционални свойства. Всичко оборудване за галванично покритиеспоред степента на механизация се класифицира на:
- механизирани линии с напълно автоматично управление;
- с възможност за частично ръчно управление;
- напълно ръчни линии;
- мини линии.

Комплектът за доставка на линията, в зависимост от нейния модел, освен вани включва:
- транспортни системи (автооператори, манипулатори);
- промишлено и местно оборудване за пречистване на отпадъчни води;
- спомагателно оборудване: устройства за поцинковане (окачвания, камбани, барабани), катодни и анодни пръти, топлообменници, нагревателни елементи и др.;
- допълнително оборудване: вентилационна система, токоизправителни агрегати, компресори и вентилатори, хладилно оборудване, сушилни камери и шкафове, помпи, оборудване за производство на полуводни, филтриращи агрегати;
- и други.
5 Електролити, използвани при поцинковане
В галваничното производство, въз основа на предназначението на продукта, се използват различни електролити за поцинковане. Те са условно разделени на 2 основни групи:
- Прости киселинни (хлорид, сулфат, хидроборен флуорид) - в тях цинкът е хидратиран йон.
- Комплексен комплекс (цинкат, цианид, пирофосфат, амоняк и други) - цинкът присъства в състава на комплексните йони, които са положително или отрицателно заредени. Тези електролити за поцинковане се разделят на киселинни и алкални.
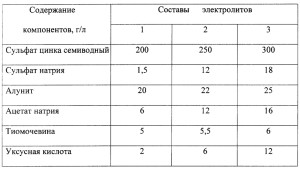
Съставът и естеството на електролитите за поцинковане зависят от скоростта на отлагане и качеството на цинковите отлагания върху катода.
Най-популярният метод за покритие е в леко кисели прости електролити за поцинковане.Те позволяват използването на ток с по-висока плътност от сложните и съответно се отличават с по-висока скорост на процеса на растеж на покритието. Галваничното покритие с тези електролити за поцинковане също се характеризира с високо ниво на покритие и добро външен видполучените покрития. Стоманата, когато се използва, е по-малко податлива на хидрогениране, което води до крехкост на частите. Но тези електролити са подходящи само за заготовки с проста конфигурация, тел, лента. Качеството на покритията не е много високо.

Отлагането на цинк от сложни електролити за цинково покритие протича при условия на високо йонно разсейване, с намаляване на добива на метал и увеличаване на отделянето на водород с увеличаване на плътността на тока. Следователно тези решения се използват с ниска плътност на тока. Използването им дава възможност за получаване на фино-зърнести, равномерни, много висококачествени покрития върху продукти както с прости, така и със сложни форми.





