Esența anodică de protecție împotriva coroziunii. Opțiuni pentru protecția catodică a conductelor - avantaje și dezavantaje ale metodelor. Motive pentru protecția benzii de rulare
Toate metodele care prelungesc durata de viață a conductei pot fi împărțite în patru grupuri.
Apărare pasivă . Constă în aplicarea unui strat protector izolator pe bază de bitum, benzi polimerice sau polimer pulverizat pe suprafața țevii. Straturile izolante trebuie să aibă continuitate, capacitate dielectrică mare, aderență, rezistență mecanică, rezistență la apă, elasticitate, biostabilitate, rezistență la căldură, durabilitate și nedeficiență.
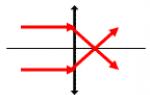
Ei prepară un amestec fierbinte de apă sărată, o soluție apoasă de hexacianoferat de potasiu, fenolftaleină și un agent de gelifiere. Se toarnă acest amestec în două vase Petri și se lasă să se răcească timp de o oră până când gelul îngheață. Se observă că părțile extreme ale unghiei sunt înconjurate de o zonă albastră, iar partea centrală este înconjurată de o zonă roz. Ce ioni au apărut în părțile extreme și în partea centrală a unghiei?
Scrieți o semi-ecuație electronică care translată metalul metalic de la capetele unghiei. Este scrisă o semiecuație electronică care traduce transformarea care are loc în partea centrală a unghiei. Pentru a interpreta observațiile făcute în placa Petri, se presupune că unghia se comportă ca un micropil, deoarece oxidarea și reducerea au loc în zone separate. Ca în orice celulă convențională, neutralitatea electrică a mediului este asigurată de deplasarea ionilor aici în gelul de sare. Completați figura 1 subliniind.
Introducere în metal a componentelor care cresc rezistența la coroziune . Metoda se aplică în etapa de fabricare a metalului. În același timp, impuritățile care reduc rezistența la coroziune sunt îndepărtate din metal.
Impact asupra mediului . Metoda se bazează pe introducerea inhibitorilor de coroziune pentru a dezactiva mediul agresiv.
Zone de oxidare și reducere, zone anodice și catodice. . Unghia este inconjurata de o zona roz aproape uniforma, in timp ce foaia de zinc este inconjurata de o zona alba. Care este unul dintre cele două metale oxidat? Utilizați rezultatele acestui experiment pentru a explica de ce constructorii de nave atașează blocuri de zinc pe corpul de oțel al navelor.
Protectie cu invelis metalic: electrozincare
Marinarul vrea să ofere protectie buna carena navei dumneavoastră prin acest proces. Pentru a face acest lucru, el conectează un voltmetru în mod continuu între carcasa de oțel și blocul de zinc. Una dintre metodele folosite pentru a proteja oțelul de coroziune este izolarea acestuia de atmosferă prin acoperirea acestuia cu un strat de metal, astfel încât plăcile de oțel să fie acoperite cu un strat subțire de zinc. că sunt „zincate”.
Protecție activă . Această metodă include protecția catodică, a benzii de rulare și a drenajului.
48. Protectie catodica
Cu protecția catodică a conductei, polul pozitiv al sursei de curent continuu (anod) este conectat la un electrod de împământare anod special, iar negativul (catodul) este conectat la structura protejată (Fig. 2.24).
Orez. 2.24. Schema de protecție catodică a conductelor
În această baie electrolitică, placa de acoperit este scufundată, iar ca al doilea electrod se folosește o placă de zinc. Placa de oțel are o suprafață totală de 10 m 2. Este de dorit să se aplice un strat de zinc de 0,10 mm grosime, care corespunde unui volum de zinc egal cu 1,0 × 10 3 cm 3 l. Intensitatea curentului se menține constantă și egală. la 1,0 kA.
Funcționarea unui experiment efectuat într-o cutie Petri
Semiecuația electronică corespunzătoare. Cele două semiecuații de electroni pentru oxidarea fierului metalic și pentru reducerea oxigenului se adaugă prin atribuirea unui factor de 2 oxidării, astfel încât electronii vânduți în timpul oxidării să compenseze electronii capturați în timpul reducerii.
1- linie de alimentare;
2 - punct transformator;
3 - statie de protectie catodica;
4 - conductă;
5 - împământare anod;
6 - cablu
Principiul de funcționare al protecției catodice este similar cu electroliza. Sub influența unui câmp electric, începe mișcarea electronilor de la sistemul electrod de împământare anod către structura protejată. Pierzând electroni, atomii de metal ai electrodului de împământare anodului trec sub formă de ioni în soluția de electrolit din sol, adică electrodul anodului este distrus. La catod (conducta) se observă un exces de electroni liberi (recuperarea metalului structurii protejate).
Conform semi-ecuației electronice, mol. Protecția catodă este o metodă activă anticorozivă care elimină riscul de coroziune a structurilor din beton înglobat, scufundat sau armat. Astfel, protectia catodica face posibila perpetuarea instalatiilor, limitarea riscurilor de evacuare, afectand astfel mediul.
Protecția catodică este de a trimite o continuă curent electricîntr-o structură care se poate coroda, poate fi îngropată sau scufundată. Introducerea de curent în structura protejată face posibilă reducerea potențialului său electrochimic sub o valoare predeterminată. Acest potențial depinde, parțial, de natura metalului și de mediul în care este scufundat.
49. Protectia benzii de rulare
Când se instalează conducte în zone greu accesibile, îndepărtate de sursele de energie, se folosește protecția benzii de rulare (Fig. 2.25).

1 - conductă;
2 - protector;
3 - conductor;
4 - coloana de control
În cazul fierului, componenta principală a oțelului, zona albastră reprezintă zona de imunitate, adică potențialul și valorile pH-ului pentru care oțelul nu se va oxida. unul in care se va oxida si va fi stabil sub forma de ioni in solutie, iar in final zona portocalie, otelul este format din straturi oxidante de oxizi de protectie, apoi rata sa de coroziune este mai mica.
Când un metal se corodează, se creează două zone distincte la interfața cu mediul coroziv. Zona din care curge curentul, metalul se dizolvă sau apa conținută în mediu este oxidată, electronii sunt eliberați în metal, se numește anod. Zona în care intră fluxurile, vederea în soluție este redusă prin captarea electronilor furnizați de anod, se numește catod.
Orez. 2.25. Sistem protectia benzii de rulare
Principiul de funcționare al protecției sacrificiale este similar cu cel al unui cuplu galvanic. Doi electrozi - o conductă și un protector (făcut dintr-un metal mai electronegativ decât oțelul) sunt conectați printr-un conductor. În acest caz, apare o diferență de potențial, sub acțiunea căreia există o mișcare direcționată a electronilor de la anodul protector la catodul conductei. Astfel, protectorul este distrus, nu conducta.
În cazul coroziunii generalizate, aceste două zone se deplasează aleatoriu pe suprafața metalului, coroziunea ajunge uniform pe întreaga suprafață. În cazul coroziunii localizate, aceste două zone nu se mișcă, coroziunea pătrunde rapid în metal și îl slăbește rapid.
Două tehnologii de protecție catodică sunt utilizate pentru a furniza curentul necesar pentru a rezista fenomenelor de coroziune. Anozii de sacrificiu sau galvanici: funcționează datorită cuplajului galvanic creat în mod natural între metalul structurii și anozi, constând din aliaje de zinc, aluminiu sau magneziu, metale mai electronegative, diferența naturală de potențial dintre metale creează o circulație de curent, potenţialul de lucru scade şi potenţialul anodic creşte . Lucrarea este mai catodica, deci se corodeaza mai putin repede decat daca ar fi singur sau chiar mai mult, iar anozii se corodeaza mult mai repede decat daca ar fi singuri. Curent suprapus: stația de ieșire generează DC. care curge între structură și barajul anodic, format din anozi îngropați sau scufundați. Curentul iese din anozi și intră în structură pentru a-și reduce potențialul electrochimic. Sursele de energie pentru acest sistem pot fi stații alimentate dintr-o rețea de distribuție convențională, sau pentru panouri solare de putere redusă sau baterii de mare capacitate. Ele nu sunt neapărat distruse, spre deosebire de anozii de sacrificiu. . intermitent galvanizare la cald.
Materialul benzii de rulare trebuie să îndeplinească următoarele cerințe:
Asigurați cea mai mare diferență de potențial între metalul protector și oțel;
Curentul la dizolvarea unei unități de masă a protectorului ar trebui să fie maxim;
Raportul dintre masa benzii de rulare utilizată pentru a crea un potențial de protecție și masa totală a benzii de rulare ar trebui să fie cel mai mare.
Aplicarea industrială a galvanizării la cald se desfășoară de aproape două secole. Cu toate acestea, acest proces rămâne cel mai mult mod eficient protejați oțelul de rugină. În ciuda îmbunătățirilor tehnice semnificative de-a lungul timpului, galvanizarea constă în continuare în scufundarea pieselor de oțel într-o baie de zinc topit.
Ceea ce distinge galvanizarea la cald de alte sisteme de protecție este că atunci când piesa de prelucrat este în contact cu zincul la temperaturi de peste 450°, pe suprafața piesei de prelucrat se formează mai multe aliaje pe bază de zinc. Pe suprafața lor se formează o „patină” în decurs de câteva luni, care este un ecran impenetrabil și rezistent împotriva agenților corozivi de mediu. Grosimea stratului de zinc este determinată în principal de grosimea peretelui oțelului, grosimea minimă necesară este inclusă în standardele actuale.
Cerințele sunt cel mai bine îndeplinite magneziu, zinc și aluminiu. Aceste metale oferă o eficiență de protecție aproape egală. Prin urmare, în practică, aliajele lor sunt utilizate cu ajutorul aditivilor îmbunătățitori ( mangan, care mărește puterea curentă și India- creşterea activităţii protectorului).
Coroziunea este unul dintre cei mai des întâlniți și, în același timp, factori distructivi care afectează o mașină în timpul funcționării. Au fost dezvoltate mai multe metode pentru a proteja corpul de acesta și există atât măsuri care vizează în mod specific acest fenomen, cât și tehnologii complexe pentru protejarea mașinii, protejând-o de diverși factori. În acest articol, este luată în considerare protecția electrochimică a corpului.
Atunci când alegeți galvanizarea la cald, este important să țineți cont de acest lucru atunci când proiectați o structură. În primul rând, trebuie să se asigure că diferitele tipuri de oțel care alcătuiesc piesa sunt potrivite pentru galvanizare și că dimensiunile piesei sunt compatibile cu dimensiunile utile ale băilor. Cooperarea strânsă cu galvanizatorul este cea mai bună garanție pentru rezultate optime.
Nu este întotdeauna posibil să se detecteze că o structură a fost galvanizată deoarece este posibil să fi fost acoperită ulterior cu un strat de vopsea, de exemplu din motive estetice. O piesă galvanizată la cald care ruginește după zeci de ani de service fiabil și fără întreținere poate fi dezinfectată și regalvanizată fără probleme; este gata să înceapă un nou ciclu de viață.
Cauzele coroziunii
Deoarece metoda electrochimică de protecție a mașinii este îndreptată exclusiv împotriva coroziunii, trebuie luate în considerare motivele care provoacă deteriorarea caroseriei. Principalele sunt apa și chimicalele rutiere folosite în perioada rece. Când sunt combinate între ele, formează o soluție salină foarte concentrată. În plus, murdăria care s-a depus pe corp reține umezeala în pori pentru o perioadă lungă de timp, iar dacă conține reactivi de drum, atrage și molecule de apă din aer.
Proiecte
Bobina laminată la cald sau la rece poate fi acoperită cu un strat protector metalic. cele mai cunoscute procese.
Zincare la cald continuu
Zincare continuă la cald: bobina laminată la cald sau la rece este scufundată într-o baie de zinc. Următoarele acoperiri sunt disponibile în acest proces de protecție.galvanizare electrolitică
Galvanizare electrolitică: se aplică un strat de zinc prin diferența de potențial anodic dintre banda laminată la rece și baia de zinc. Un strat de acoperire organic poate fi aplicat pe bobinele laminate la rece. Sunt disponibile mai multe tipuri de acoperire și o gamă largă de culori. De regulă, bobinele preacoperite sunt apoi profilate în elemente de acoperiș și fațade de diferite forme și dimensiuni.
Situația se agravează dacă vopseaua mașinii prezintă defecte, chiar și de dimensiuni reduse. În acest caz, răspândirea coroziunii va avea loc foarte rapid și chiar și straturile de protecție conservate sub formă de grund și galvanizare ar putea să nu oprească acest proces. Prin urmare, este important nu numai să curățați constant mașina de murdărie, ci și să monitorizați starea vopselei sale. Fluctuațiile de temperatură, precum și vibrațiile joacă, de asemenea, un rol în răspândirea coroziunii.
Termenul „electroliza” se referă la fenomenele naturale de coroziune galvanică și accidentală a coroziunii electrolitice prin abuzul de limbaj și în condiții de yachting. Coroziunea metalelor este un fenomen electrochimic: implică curenți electrici măsurabili și afectează atât siguranța echipajelor, cât și valoarea ambarcațiunilor afectate.
Coroziunea metalelor este ușoară
Coroziunea rezultă din circulația curentului electric, natural sau suprapus, între anod și catodul conducător de legătură și scufundat în același electrolit. Există distrugere materială la anod și protecție la catod, de unde și termenul de protecție catodică.
De asemenea, trebuie menționate zonele mașinii care sunt cele mai susceptibile la deteriorarea coroziunii. Acestea includ:
- părțile cele mai apropiate de suprafața drumului, adică praguri, aripi și sub caroserie;
- suduri rămase după reparație, mai ales dacă a fost efectuată analfabet. Acest lucru se datorează „slăbirii” la temperatură ridicată a metalului;
- în plus, rugina afectează adesea diverse cavități ascunse prost ventilate, unde umiditatea se acumulează și nu se usucă mult timp.

Coroziunea galvanică și coroziunea electrolitică
Coroziunea galvanică este legată de diferențele naturale de potențial existente între diferite metale aflate în contact în același electrolit la începutul circulației unui curent electric de intensitate foarte mică: curentul de coroziune. Rezistă eficient anozii de sacrificiu, care oferă în mod natural un curent de protecție care contracarează fluxul de coroziune. Atentie, protectia catodica pe care o asigura nu este asumata: masurata!
Principiul de funcționare a protecției electrochimice
Metoda considerată de protejare a corpului de rugină este denumită metode active. Diferența dintre ei și moduri pasive constă în faptul că cele dintâi creează orice măsuri de protecție care nu permit factorilor de coroziune să afecteze mașina, în timp ce cele din urmă doar izolează caroseria de efectele aerului atmosferic. Această tehnologie a fost utilizată inițial pentru protecția împotriva ruginii a conductelor și a structurilor metalice. Metoda electrochimică este considerată una dintre cele mai eficiente.
Pe de altă parte, coroziunea electrolitică se datorează prezenței unui curent continuu și aleator: un curent de scurgere care crește într-o direcție sau alta și în funcție de polaritatea sa - impactul curentului de coroziune. Atenție, curenții de scurgere nocivi de pe margine sau terasament tind întotdeauna să ajungă la „pământ” și să provoace coroziune accelerată a metalului conductor la punctele de ieșire în mare! Anozii nu ajută atunci și numai detectarea timpurie și neutralizarea rapidă a unor astfel de curenți vă vor salva de consecințele lor costisitoare!
Această metodă de protecție a corpului, numită și catodă, se bazează pe caracteristicile cursului reacțiilor redox. Concluzia este că o sarcină negativă este aplicată pe suprafața protejată.
Schimbarea potențialului se realizează folosind o sursă de curent continuu externă sau prin conectarea la un anod de sacrificiu, constând dintr-un metal mai electronegativ decât obiectul protejat.
Potențialul de coroziune și protecția metalelor subacvatice
Protecția metalelor scufundate împotriva coroziunii este asigurată în comun de sistemul de vopsire, precum și de sistemul de protecție catodică. Eficacitatea acestuia depinde de valoarea atinsă de potențialul lor de coroziune, exprimată în mV. În imaginea temperaturii corpului uman, controlul acesteia cu ajutorul unui dispozitiv adecvat se realizează folosind o măsurătoare simplă, a cărei interpretare este instantanee: potențialul de coroziune trebuie să fie în intervalul de protecție. Valoarea acestuia indică nivelul de protecție asigurat de anozi, care este un rol esențial, și vă avertizează, dacă este necesar, despre posibila prezență a curenților nocivi de scurgere de margine sau de andocare.
Principiul de funcționare al protecției electrochimice a mașinii este acela că între suprafața corpului și suprafața obiectelor din jur, datorită diferenței de potențial dintre acestea, trece un curent slab prin circuitul reprezentat de aer umed. În astfel de condiții, metalul mai activ suferă oxidare, în timp ce celălalt, dimpotrivă, este redus. De aceea plăcile de protecție din metale electronegative folosite pentru automobile se numesc anozi de sacrificiu. Cu toate acestea, cu o deplasare excesivă a potențialului în direcția negativă, degajarea hidrogenului, modificarea compoziției stratului apropiat de electrod și alte fenomene care duc la degradarea învelișului de protecție și la apariția coroziunii la stres a stratului protejat. obiect sunt posibile.
Tehnologia luată în considerare pentru mașini implică utilizarea unei caroserie ca catod (stâlp încărcat negativ), iar diferite obiecte sau elemente înconjurătoare instalate pe mașină care conduc curentul, de exemplu, structuri metalice sau suprafețe ude ale drumului, servesc drept anozi (pozitiv poli încărcați). În acest caz, anodul trebuie să fie format dintr-un metal activ, cum ar fi magneziu, zinc, crom, aluminiu.

Multe surse indică diferența de potențial dintre catod și anod. În conformitate cu acestea, pentru a crea o protecție completă împotriva coroziunii pentru fier și aliajele sale, este necesar să se atingă un potențial de 0,1-0,2 V. Valorile mari au un efect redus asupra gradului de protecție. În acest caz, densitatea curentului de protecție ar trebui să fie între 10 și 30 mA/m².
Cu toate acestea, aceste date nu sunt în întregime corecte - în conformitate cu legile electrochimiei, distanța dintre catod și anod este direct proporțională cu mărimea diferenței de potențial. Prin urmare, în fiecare caz specific, este necesar să se obțină o anumită valoare a diferenței de potențial. În plus, aerul, considerat în acest proces ca un electrolit, este capabil să conducă un curent electric caracterizat printr-o diferență mare de potențial (aproximativ kW), prin urmare, un curent cu o densitate de 10-30 mA/m² nu va fi condus de către aer. Numai un curent „lateral” poate apărea ca urmare a udării anodului.
În ceea ce privește diferența de potențial, se observă polarizarea concentrației față de oxigen. În același timp, moleculele de apă care au căzut pe suprafața electrozilor sunt orientate spre ei în așa fel încât electronii să fie eliberați, adică o reacție de oxidare. La catod, această reacție, dimpotrivă, se oprește. Datorită absenței curentului electric, eliberarea electronilor este lentă, astfel încât procesul este sigur și invizibil. Datorită efectului polarizării, există o schimbare suplimentară a potențialului corpului în direcția negativă, ceea ce face posibilă oprirea periodică a dispozitivului de protecție împotriva coroziunii. Trebuie remarcat faptul că zona anodului determină direct proporțional eficiența protecției electrochimice.

Opțiuni de creare
În orice caz, rolul catodului va fi îndeplinit de caroseria mașinii. Utilizatorul trebuie să selecteze un obiect care va fi folosit ca anod. Alegerea se face pe baza condițiilor de funcționare ale mașinii:
- Pentru mașinile care sunt staționare, un obiect metalic din apropiere, cum ar fi un garaj (cu condiția să fie construit din metal sau să aibă elemente metalice), o buclă de pământ care poate fi instalată în absența unui garaj într-o parcare deschisă, este potrivită ca un catod.
- Pe o mașină în mișcare, pot fi utilizate dispozitive precum o „coadă de împământare metalizată din cauciuc”, protectori (electrozi de protecție) montați pe caroserie.
Datorită absenței curentului care curge între electrozi, este suficient să conectați rețeaua de bord a mașinii de +12 volți la unul sau mai mulți anozi printr-un rezistor suplimentar. Acest din urmă dispozitiv servește la limitarea curentului de descărcare a bateriei în cazul unui scurtcircuit anod-catod. Principalele motive pentru scurtcircuit sunt instalarea analfabetă a echipamentelor, deteriorarea anodului sau descompunerea chimică a acestuia din cauza oxidării. În plus, sunt luate în considerare caracteristicile utilizării articolelor enumerate anterior ca anozi.
Utilizarea unui garaj ca anod este considerată cel mai mult într-un mod simplu protecția electrochimică a caroseriei unei mașini în picioare. Dacă camera are o podea metalică sau o pardoseală cu secțiuni deschise de fitinguri din fier, atunci va fi asigurată și protecția fundului. În perioada caldă, în garajele metalice se observă un efect de seră, cu toate acestea, în cazul creării unei protecții electrochimice, aceasta nu distruge mașina, ci mai degrabă are ca scop protejarea corpului de coroziune.
Este foarte simplu să creezi protecție electrochimică în prezența unui garaj metalic. Pentru a face acest lucru, este suficient să conectați acest obiect la conectorul pozitiv al bateriei mașinii printr-un rezistor suplimentar și un fir de montare.
Chiar și bricheta poate fi folosită ca conector pozitiv, cu condiția ca acesta să existe tensiune atunci când contactul este oprit (nu pentru toate mașinile acest dispozitiv rămâne funcțional când motorul este oprit).

La crearea protecției electrochimice, bucla de împământare este folosită ca anod conform aceluiași principiu ca și garajul metalic discutat mai sus. Diferența este că garajul protejează întreaga caroserie a mașinii, în timp ce această metodă este doar fundul acesteia. Bucla de pământ este creată prin introducerea a patru tije metalice de cel puțin 1 m lungime în pământ în jurul perimetrului mașinii și tragerea unui fir între ele. Circuitul este conectat la mașină, precum și la garaj, printr-o rezistență suplimentară.
„Coada” de împământare metalizată din cauciuc este cel mai simplu mod de protecție electrochimică a unei mașini în mișcare împotriva coroziunii. Acest dispozitiv este o bandă de cauciuc cu elemente metalice. Principiul funcționării sale este că în condiții de umiditate ridicată apare o diferență de potențial între caroserie și suprafața drumului. Mai mult, cu cât umiditatea este mai mare, cu atât eficiența protecției electrochimice creată de elementul în cauză este mai mare. „Coada” de împământare este instalată în spatele mașinii astfel încât să fie stropită cu apă care zboară de sub roata din spate atunci când conduceți pe un drum umed, deoarece aceasta crește eficiența protecției electrochimice.
Avantajul cozii de împământare este că, pe lângă funcția de protecție electrochimică, eliberează caroseria mașinii de tensiunea statică. Acest lucru este valabil mai ales pentru vehiculele care transportă combustibil, deoarece scânteia electrostatică, care este rezultatul acumulării unei sarcini statice în timpul mișcării, este periculoasă pentru încărcătura transportată de aceasta. Prin urmare, dispozitivele sub formă de lanțuri metalice care târăsc de-a lungul suprafeței drumului se găsesc, de exemplu, pe camioanele cu combustibil.

În orice caz, este necesar să izolați coada de împământare de caroseria mașinii în curent continuu și, invers, „scurt” în curent alternativ. Acest lucru se realizează prin utilizarea unui lanț RC, care este un filtru de frecvență elementar.
Protecția mașinii împotriva coroziunii cale electrochimică cu utilizarea electrozilor de protecție ca anozi, este proiectat și pentru funcționarea în mișcare. Protecțiile sunt instalate în locurile cele mai vulnerabile la coroziune ale corpului, reprezentate de praguri, aripi, fund.
Electrozii de protecție, ca în toate cazurile considerate anterior, funcționează pe principiul creării unei diferențe de potențial. Avantajul acestei metode este prezența constantă a anozilor, indiferent dacă mașina este în picioare sau în mișcare. Prin urmare, această tehnologie este considerată foarte eficientă, dar este cea mai dificil de creat. Acest lucru se explică prin faptul că, pentru a asigura o eficiență ridicată a protecției, este necesară instalarea a 15-20 de protecție pe caroseria mașinii.
Ca electrozi de protecție, elemente din materiale precum aluminiu, oţel inoxidabil, magnetit, platină, carboxil, grafit. Primele două opțiuni sunt clasificate ca se prăbușesc, adică electrozii de protecție alcătuiți din ei trebuie schimbați la intervale de 4-5 ani, în timp ce restul sunt numiți nedistructivi, deoarece se caracterizează printr-o durabilitate semnificativ mai mare. În orice caz, protectorii sunt plăci rotunde sau dreptunghiulare cu o suprafață de 4-10 cm².
În procesul de creare a unei astfel de protecție, este necesar să se țină cont de unele caracteristici ale protectorilor:
- raza acțiunii de protecție se extinde până la 0,25-0,35 m;
- electrozii trebuie instalați numai pe zonele care au vopsea;
- pentru a fixa elementele în cauză, folosiți clei epoxidic sau chit;
- se recomandă curățarea luciului înainte de instalare;
- este inacceptabil să acoperiți partea exterioară a protectorilor cu vopsea, mastic, lipici și alte substanțe electroizolante;
- deoarece electrozii de protecție sunt plăci de condensatoare încărcate pozitiv, aceștia trebuie să fie izolați de suprafața încărcată negativ a caroseriei mașinii.

Rolul garniturii dielectrice a condensatorului va fi îndeplinit de vopseaua și lipiciul situat între protectori și caroseria mașinii. De asemenea, trebuie luat în considerare faptul că distanța dintre protectori este direct proporțională cu câmpul electric, astfel încât acestea trebuie instalate la o distanță mică unul de celălalt pentru a asigura o capacitate suficientă a condensatorului.
Firele către electrozii de protecție sunt conduse prin perforațiile din dopurile de cauciuc care închid găurile din fundul mașinii. Este posibil să instalați mai multe dispozitive de protecție mici sau mai puțini electrozi de protecție mai mari pe vehicul. În orice caz, este necesar să se utilizeze aceste elemente în zonele cele mai vulnerabile la coroziune, cu fața spre exterior, deoarece rolul electrolitului în acest caz este jucat de aer.
După instalarea acestui tip de protecție electrochimică, caroseria mașinii nu va fi șocată, deoarece creează electricitate cu o forță foarte mică. Chiar dacă o persoană atinge electrodul de protecție, nu va primi o lovitură. Acest lucru se explică prin faptul că în protecția electrochimică anticoroziune se folosește un curent continuu de putere redusă, care creează un câmp electric slab. În plus, există o teorie alternativă, conform căreia câmpul magnetic există doar între suprafața corpului și locul unde sunt instalați electrozii de protecție. Prin urmare, câmpul electromagnetic creat protectie electrochimica, de peste 100 de ori mai slab decât câmpul electromagnetic al unui telefon mobil.