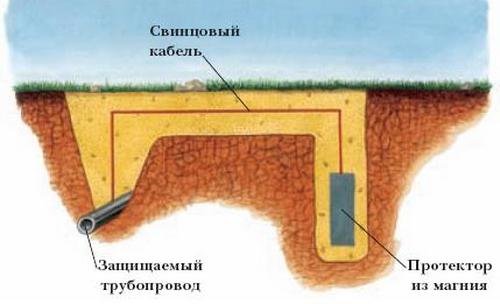
Schéma ochranné ochrany proti korozi. Přechod v řadě provedení z kovu. Negativní vliv elektrochemické koroze
Elektrochemická ochrana – účinná metoda ochrana hotových výrobků před elektrochemickou korozí. V některých případech je nemožné obnovit lak nebo ochranný obalový materiál, pak je vhodné použít elektrochemickou ochranu. Nátěr podzemního potrubí nebo dna námořního plavidla je velmi pracný a nákladný na obnovu, někdy je to prostě nemožné. Elektrochemická ochrana spolehlivě chrání výrobek před korozí, zabraňuje zničení podzemních potrubí, dna lodí, různých nádrží atd.
Vzhledem k zásadní důležitosti diskutovaného problému byl zahájen výzkum nové generace levných povlaků odolných proti chromu, které lze široce používat pro ochranu proti vysokoteplotní korozi. Inovativnost navrženého řešení se projevuje v nátěrech s nízkou tloušťkou. Oxidační studie byly prováděny při konstantní teplotě a také za podmínek tepelného šoku.
Chromové povlaky byly získány pomocí magnetronového naprašování. Bylo zjištěno, že povrchy modifikačních ventilů se staly odolnými vůči oxidaci. Konference se konala dne anglický jazyk se simultánním překladem celého kurzu do polštiny.
Platí elektrochemická ochrana v případech, kdy je možnost volné koroze v oblasti intenzivního rozpouštění základního kovu nebo nadměrné pasivace. Tito. kdy dochází k intenzivní destrukci kovové konstrukce.
Podstata elektrochemické ochrany
dokončit kovový výrobek stejnosměrný proud je připojen zvenčí (zdroj stejnosměrný proud nebo ochránce). Elektrický proud na povrchu chráněného výrobku vytváří katodickou polarizaci elektrod mikrogalvanických párů. Výsledkem toho je, že anodické oblasti na kovovém povrchu se stanou katodickými. A v důsledku vystavení koroznímu prostředí není zničen kov konstrukce, ale anoda.
Zúčastnilo se ho více než 150 malířů a vědců z 19 zemí a zúčastnilo se jej více než 100 institucí, z nichž více než 80 % tvořily průmyslové celky. Na začátku se zaměřujeme především na technické a finanční aspekty projektu. Při provádění antikorozní ochrany problémy životního prostředí minimalizace kontaminace během tryskání a nanášení barvy. V případě antikorozních prací je to velmi důležité kvůli použití materiálů, které jsou zvláště nebezpečné pro životní prostředí.
Podle toho, kterým směrem (kladným nebo záporným) se potenciál kovu posouvá, se elektrochemická ochrana dělí na anodu a katodu.
Katodická ochrana proti korozi
Katodická elektrochemická ochrana proti korozi se používá, když chráněný kov není náchylný k pasivaci. Jedná se o jeden z hlavních typů ochrany kovů před korozí. Podstatou katodické ochrany je aplikace vnějšího proudu ze záporného pólu na výrobek, který polarizuje katodické úseky korozních prvků a přibližuje hodnotu potenciálu anodovým. Kladný pól zdroje proudu je připojen k anodě. V tomto případě se koroze chráněné konstrukce sníží téměř na nulu. Anoda se postupně ničí a musí být pravidelně vyměňována.
Ne vždy však víme, že investice mohou být vážnou hrozbou kvůli okolní přírodě, zejména kvůli okolnímu ptactvu. Inženýrské stavby jsou atraktivním místem pro vytváření nových ptačích stanovišť. Vzhledem k tomu, že nejvhodnější období pro provádění antikorozních prací v terénu „se kryje“ s obdobím země ptactva, máme co do činění s „střetem zájmů“. Ptáci obývající inženýrské objekty velmi často patří k chráněným druhům, což povede k problému. Stavba nového inženýrské stavby Výstavba nových inženýrských staveb je podnik, který může významně ovlivnit životní prostředí a v souladu se zákonem o ochraně životního prostředí je v takovém případě nutné získat tzv. rozhodnutí o podmínkách životního prostředí.
Existuje několik možností katodické ochrany: polarizace z vnějšího zdroje elektrického proudu; snížení rychlosti katodového procesu (například odvzdušnění elektrolytu); kontakt s kovem, který má v daném prostředí více elektronegativní potenciál pro volnou korozi (tzv. obětní ochrana).
Povinnost získat toto rozhodnutí náleží investorovi a musí být přijata před přijetím dalších rozhodnutí nezbytných pro investici. Ptáci jsou důležitým prvkem prostředí, které nás obklopuje, a proto je nutné toto zahrnout do ekologického řešení. Článek prezentuje vliv domovních odpadních vod na betonové skruže, které byly použity k výstavbě čerpacích stanic. Zkoušky byly provedeny na vzorcích betonu a betonových korozních produktů, které byly odebrány ze stávajících a fungujících kanalizačních studní.
Polarizace z vnějšího zdroje elektrického proudu se používá velmi často k ochraně konstrukcí umístěných v půdě, vodě (dna lodí apod.). kromě tento druh protikorozní ochrana se používá pro zinek, cín, hliník a jeho slitiny, titan, měď a její slitiny, olovo, ale i vysokochromové, uhlíkové, legované (nízko i vysokolegované) oceli.
Problém degradace betonu se dotkl několika vrtů celého systému čištění odpadních vod a v této vadné ventilaci. Autoři poukazují na to, že nedostatečná ventilace může být potenciálním důvodem, proč je mikroklima vůči betonu vysoce agresivní. Studie využívala výzkum chemické analýzy betonu a také mikroskopická pozorování. Kromě toho byly provedeny pevnostní zkoušky betonu pro zjištění vlivů a rozsahu pozorovaných změn v důsledku biologické koroze z hlediska změn mechanických vlastností.
Vnějším zdrojem proudu jsou stanice katodové ochrany, které se skládají z usměrňovače (konvertoru), přívodu proudu do chráněné konstrukce, anodových zemnících elektrod, referenční elektrody a anodového kabelu.
katodická ochrana aplikované jak samostatně, tak další pohled ochrana proti korozi.
Hlavním kritériem, podle kterého lze posuzovat účinnost katodické ochrany, je ochranný potenciál. Ochranný potenciál je potenciál, při kterém dochází k rychlosti koroze kovu jisté podmínky prostředí má nejnižší (pokud možno) hodnotu.
Klíčová slova: dobře, síranová koroze, síranové bakterie. Povlaky byly charakterizovány studiem jejich morfologie, chemické složení tloušťka a drsnost, stejně jako odolnost proti korozi povrchově modifikované slitiny. Byl prokázán pozitivní vliv přítomnosti fluoridu v oxidové vrstvě na korozní odolnost vzorků slitin. Povlaky byly získány chemickou depozicí z plynné fáze s plazmovým substrátem vytvořeným pomocí radiofrekvenčních elektromagnetických vln.
Je třeba zdůraznit, že vyšší teploty motoru a používání alternativních paliv výrazně urychlují degradaci jednotlivých součástí motoru a zejména výfukových ventilů motoru. Je dobře známo, že může být náchylný k průniku chloridů. Proces chlorace je předmětem mnoha prací. Hlavním tématem těchto studií je: koroze železobetonové výztuže a vliv chloridů, chemická interakce mezi iony a cementovou matricí. Úprava úpravou úpravou provedl provedl provedl provedl provedl provedl provedl provedl provedl Klíčová slova: fyzikální vlastnosti, beton, vápenné kamenivo, chloridové médium, okolní teplota.
Použití katodové ochrany má nevýhody. Jedním z nich je nebezpečí přehnaná ochrana. Nadměrná ochrana je pozorována s velkým posunem potenciálu chráněného objektu v negativním směru. Zároveň vyniká. Výsledkem je zničení ochranných povlaků, vodíkové křehnutí kovu, korozní praskání.
Je známo, že cementový beton může být náchylný k pronikání chloridů. Popis tohoto jevu pro cementový beton vyrobený z nereaktivní štěrkové rudy byl již předmětem četných prací. V práci byly zohledněny výhody metody a některé nepříjemnosti, které se dosud nepodařilo odstranit. Výše uvedené účinky koroze způsobují systematický pokles únosnosti železobetonových prvků, proto hraje významnou roli hodnocení koroze výztuže. Po určení nebezpečí koroze výztuže v testovaném provedení musíte okamžitě rozhodnout o konkrétní sanaci.
Ochrana běhounu (aplikace běhounu)
Typ katodické ochrany je katodická ochrana. Použitím ochrana běhounu k chráněnému předmětu je připojen kov s více elektronegativním potenciálem. V tomto případě není zničena konstrukce, ale běhoun. Protektor časem koroduje a je nutné jej vyměnit za nový.
Kromě vizuálního posouzení byl také kvantifikován postup korozního procesu. Úvod Ocel je důležitý konstrukční materiál použitelný v mnoha průmyslových odvětvích. V mnoha případech je však důležité správně chránit ocelové povrchy prvků před korozí. Jedním ze způsobů ochrany oceli před korozí je použití kovových povlaků s anodovým charakterem.
V případě galvanického článku je tento povlak anodou a prochází destruktivními oxidačními procesy; substrátem v tomto systému je katoda a nekoroduje. Některé z nejlepších anodických povlaků zahrnují elektrolytické zinkové povlaky s kovy skupiny železa, tj. nikl, kobalt a železo. Povlaky tohoto typu se vyrábějí elektrolyticky. V průmyslu je často nutné maskovat části ocelových výrobků nanesením vrstvy mědi na povrch. Tato vrstva se pak nejčastěji odstraňuje leptáním v roztocích kyseliny chromové, což představuje obrovské ohrožení životního prostředí.
Ochrana běhounu je účinná v případech, kdy je mezi chráničem a okolím malý přechodový odpor.
Každý chránič má svůj ochranný rádius, který je určen maximem možná vzdálenost, na kterém lze chránič sejmout bez ztráty ochranného účinku. Ochranná ochrana se používá nejčastěji, když je nemožné nebo obtížné a nákladné přivést do konstrukce proud.
Práce analyzovala možnost použití roztoků obsahujících peroxid vodíku jako oxidačního činidla a sloučenin obsahujících komplexy mědi. Na základě analýzy fyzikálně-chemických dat byla jako potenciální komplex vybrána kyselina ethylendiamintetraoctová. Experimenty ukázaly, že roztoky obsahující tuto sloučeninu, stejně jako amoniak a peroxid vodíku, jsou ideální pro leptání mědi z povrchu oceli. Rychlost leptání mědi je v jejich případě několikanásobně vyšší než v případě roztoků kyseliny chromové, přičemž nevykazují korozivní aktivitu vůči oceli.
Chrániče se používají k ochraně konstrukcí v neutrálním prostředí (mořská nebo říční voda, vzduch, půda atd.).
Pro výrobu chráničů se používají tyto kovy: hořčík, zinek, železo, hliník. Čisté kovy neplní své ochranné funkce v plném rozsahu, proto jsou při výrobě chráničů dodatečně legovány.
Tato úprava se používá k získání povrchové vrstvy s vysokou tvrdostí při zachování pevného jádra. Nejčastěji jsou tyto vrstvy odstraněny a následně leptány v roztocích kyseliny chromové, což způsobuje ekologické problémy. Možnost nahrazení roztoků kyseliny chromové s problémy s kyslíkem. Výsledky byly doplněny studiem mikrostruktury získaných vrstev a měřením drsnosti povrchu. Získané výsledky ukázaly, že typ procesu nitrokarbonizace ovlivňuje mikrostrukturu a korozní odolnost výsledných povrchových vrstev.
Železné chrániče jsou vyrobeny z uhlíkové oceli nebo čisté železo.
Zinkové chrániče
Zinkové chrániče obsahují cca 0,001 – 0,005 % olova, mědi a železa, 0,1 – 0,5 % hliníku a 0,025 – 0,15 % kadmia. Zinkové projektory se používají k ochraně výrobků před korozí na moři (ve slané vodě). Pokud se zinkový chránič použije v mírně slané, sladké vodě nebo půdě, rychle se pokryje silnou vrstvou oxidů a hydroxidů.
Klíčová slova: nitrocenové vrstvy, slitiny titanu, korozní odolnost, Ringerův roztok Úvod Dobrý mechanické vlastnosti, velmi dobrá odolnost proti korozi v mnoha agresivních prostředích a biokompatibilita umožňují použití titanu a jeho slitin v četných lékařských aplikacích.
Vyrábí se hlavně z lékařských nástrojů a kostních a srdečních implantátů, ale kvůli přítomnosti vanadu v jeho chemii je jeho další používání zpochybňováno. Vanad je široce uznáván jako alergický a karcinogenní prvek, který způsobuje záněty. Byl diskutován způsob a technika protikorozní ochrany ocelových prvků vodních staveb provozovaných v mořské vodě, zejména v oblastech s proměnlivou hladinou vody a rozstřiky. Problém je založen na ochraně hromady ocelových hydraulických konstrukcí Severního přístavu v Gdaňsku.
Ochranný hořčík
Slitiny pro výrobu hořčíkových chráničů jsou legovány 2–5 % zinku a 5–7 % hliníku. Množství mědi, olova, železa, křemíku, niklu ve slitině by nemělo přesáhnout desetiny a setiny procenta.
Hořčíkový chránič se používá v lehce nasolených, sladké vody, půdy. Chránič se používá v prostředí, kde jsou zinkové a hliníkové chrániče neúčinné. Důležitým aspektem je, že hořčíkové chrániče je nutné používat v prostředí s pH 9,5 – 10,5. To je způsobeno vysokou rychlostí rozpouštění hořčíku a tvorbou těžko rozpustných sloučenin na jeho povrchu.
Klíčová slova: námořní vodní stavby, koroze v pásmu různých vodních stavů a rozstřiků, obnova protikorozní ochrany. Metodika a Specifikace je popsána antikorozní ochrana vod, zejména v oblastech velké vody a stříkání. Přístav se nachází v severním přístavu v Gdaňsku v Polsku. Klíčová slova: pobřežní struktury, koroze přílivu, obnova ochrany proti korozi Úvod Ocelové piloty používané při výstavbě hydraulických konstrukcí v Severním přístavu v Gdaňsku jsou v provozu již půl století.
Hořčíkový chránič je nebezpečný, protože. je příčinou vodíkového křehnutí a korozního praskání konstrukcí.
Hliníkové chrániče
Hliníkové chrániče obsahují přísady, které zabraňují tvorbě oxidů hliníku. Do takových chráničů je vloženo až 8 % zinku, až 5 % hořčíku a desetiny až setiny křemíku, kadmia, india a thallia. Hliníkové chrániče se používají v pobřežním šelfu a tekoucí mořské vodě.
Nutno zdůraznit, že antikorozní ochrana od samého počátku této piloty probíhala pouze na části povrchu v podobě živičného nátěru z ocelových trubkových pilot. Je uvedena problematika vadnosti antikorozní ochrany v oblasti nátěrů ochranných a dekorativních nátěrů provedených na ocelových prvcích svodidel dříve chráněných žárovým zinkováním. Na příkladech z různých míst se opakuje problém delaminace nátěrů bez ohledu na typ použitých nátěrových hmot a výrazný rozvoj koroze na exponovaném zinkovém podkladu.
Ochrana proti korozi anody
Anodová elektrochemická ochrana se používá pro konstrukce z titanu, nízkolegované nerezové, uhlíkové oceli, vysoce legované železné slitiny, různé pasivované kovy. Anodová ochrana se používá ve vysoce vodivém korozivním prostředí.
Pozornost byla věnována i případům porušení týkajících se stejných prvků, ale souvisejících s nedostatečným řádným dohledem při provádění antikorozních prací. Klíčová slova: prášková barva, polyesterová prášková barva, mostní objekt, mostní ochranná bariéra, nátěr na pozinkovanou ocel, duplexní ochrana, vady nátěru, chyby při realizaci žárově zinkované prvky jsou uvedeny v článku. Příklady převzaty z různých povlaků.
Rozpoznání problémů s povrchem laku. Pozor se týká i ostatních případů poškození. Klíčová slova: mostní barvy, polyesterové nátěry, mosty, nátěry, mosty, nátěry na pozinkované oceli, ochranné nátěry na mostních konstrukcích. Hlavním prvkem většiny mostních konstrukcí jsou různé typy ochranných svodidel.
S anodickou ochranou se potenciál chráněného kovu posouvá na pozitivnější stranu, dokud není dosaženo pasivního stabilního stavu systému. Výhodou anodické elektrochemické ochrany je nejen velmi výrazné zpomalení rychlosti koroze, ale také to, že se korozní produkty nedostávají do produktu a média.
Anodovou ochranu lze realizovat několika způsoby: posunutím potenciálu na kladnou stranu pomocí externího zdroje elektrického proudu nebo zavedením oxidačních činidel (nebo prvků do slitiny) do korozního prostředí, které zvyšují účinnost katodického procesu na kovový povrch.
Anodová ochrana s použitím okysličovadel je svým ochranným mechanismem podobná anodické polarizaci.
Pokud se použijí pasivační inhibitory s oxidačními vlastnostmi, přechází chráněný povrch vlivem vzniklého proudu do pasivního stavu. Patří mezi ně dichromany, dusičnany atd. Ty ale dost silně znečišťují okolní technologické prostředí.
Zavedením aditiv do slitiny (zejména dopováním ušlechtilým kovem) probíhá redukční reakce depolarizátorů probíhající na katodě s nižším přepětím než na chráněném kovu.
Pokud projdeme chráněnou strukturou elektřina, potenciál se posune kladným směrem.
Zařízení pro anodickou elektrochemickou ochranu proti korozi se skládá z externího zdroje proudu, referenční elektrody, katody a samotného chráněného předmětu.
Pro zjištění, zda je možné u určitého objektu aplikovat anodickou elektrochemickou ochranu, se snímají anodické polarizační křivky, pomocí kterých je možné určit korozní potenciál studované konstrukce v určitém korozním prostředí, resp. oblasti stabilní pasivity a proudové hustoty v této oblasti.
Pro výrobu katod se používají kovy s nízkou rozpustností, jako jsou vysoce legované nerezové oceli, tantal, nikl, olovo a platina.
Aby byla anodická elektrochemická ochrana v určitém prostředí účinná, je nutné používat snadno pasivovatelné kovy a slitiny, referenční elektroda a katoda musí být stále v roztoku, spojovací prvky musí být kvalitní.
Pro každý případ anodové ochrany je rozmístění katod navrženo individuálně.
V následujících situacích anodová ochrana byl účinný pro určitý objekt, je nutné, aby splňoval některé požadavky:
Všechno svary musí být vysoce kvalitní;
V technologickém prostředí musí materiál, ze kterého je chráněný předmět vyroben, přejít do pasivního stavu;
Počet vzduchových kapes a štěrbin by měl být omezen na minimum;
Na konstrukci by neměly být žádné nýtované spoje;
V zařízení, které má být chráněno, musí být referenční elektroda a katoda vždy v roztoku.
Pro realizaci anodové ochrany v chemickém průmyslu se často používají tepelné výměníky a válcové jednotky.
Elektrochemická ochrana anody nerezové oceli použitelné pro průmyslové sklady kyseliny sírové, roztoky na bázi čpavku, minerální hnojiva, ale i všechny druhy kolektorů, nádrží, odměrných nádrží.
Anodovou ochranu lze také použít k zabránění poškození korozí v chemických niklovacích lázních, výměnících tepla při výrobě umělých vláken a kyseliny sírové.
Koroze je proces samovolné destrukce povrchu materiálů v důsledku interakce s prostředím. Jeho příčinou je termodynamická nestabilita. chemické prvky na určité látky. Formálně podléhají korozi polymery, dřevo, keramika, pryž, ale častěji se pro ně používá termín „stárnutí“. Nejzávažnější škody způsobuje rezivění kovů, na jehož ochranu se vyvíjejí high-tech protiopatření. Ale o tom si povíme později. Vědci rozlišují chemickou a elektrochemickou korozi kovů.
Chemická koroze
Obvykle se vyskytuje, když je kovová konstrukce vystavena suchým plynům, kapalinám nebo roztokům, které nevedou elektrický proud. Podstatou tohoto typu koroze je přímá interakce kovu s agresivním prostředím. Prvky chemicky korodují během tepelného zpracování nebo v důsledku toho dlouhodobý provoz na dost vysoké teploty. To platí pro lopatky plynových turbín, armatury pro tavicí pece, součásti spalovacích motorů a tak dále. V důsledku toho se na povrchu tvoří určité sloučeniny: oxidy, nitridy, sulfidy.
Je to důsledek kontaktu kovu s kapalným prostředím schopným vést elektrický proud. Vlivem oxidace dochází v materiálu ke strukturálním změnám vedoucím ke vzniku rzi (nerozpustný produkt), případně kovové částice přecházejí do roztoku iontů.
Elektrochemická koroze: příklady
Dělí se na:
- Atmosférický, ke kterému dochází, když je na povrchu kovu kapalný film, ve kterém se plyny obsažené v atmosféře (například O 2, CO 2, SO 2) mohou rozpouštět za vzniku elektrolytických systémů.
- Kapalina, která proudí ve vodivém kapalném médiu.
- Podzemní voda, která teče pod vlivem podzemní vody.

Příčiny
Protože obvykle jakýkoli kov, který se používá pro průmyslové potřeby, není ideálně čistý a obsahuje vměstky jiné povahy, dochází k elektrochemické korozi kovů v důsledku tvorby velkého počtu zkratovaných lokálních galvanických článků na povrchu železa.
Jejich vzhled může souviset nejen s přítomností různých (zejména kovových) nečistot (kontaktní koroze), ale také s heterogenitou povrchu, defekty krystalové mřížky, mechanickým poškozením a podobně.
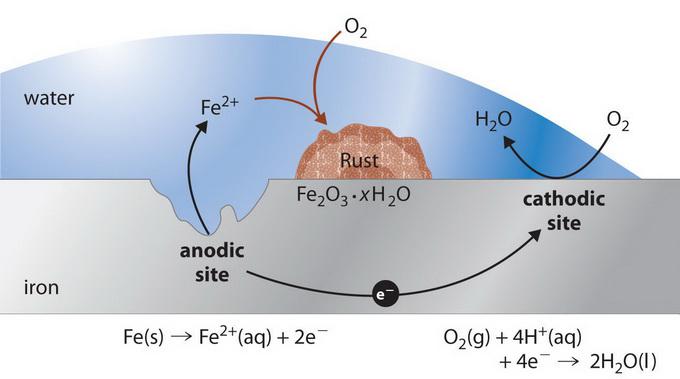
Interakční mechanismus
Proces elektrochemické koroze závisí na chemickém složení materiálů a vlastnostech vnějšího prostředí. Pokud je tzv. technický kov pokryt mokrým filmem, pak v každém z těchto galvanických mikroprvků, které se tvoří na povrchu, probíhají dvě nezávislé reakce. Aktivnější složka korozního páru daruje elektrony (například zinek v páru Zn-Fe) a přechází do kapalného prostředí jako hydratované ionty (to znamená, že koroduje) podle následující reakce (anodický proces):
M + nH20 \u003d Mz + * nH20 + ze.
Tato část povrchu je záporným pólem místního mikroelementu, kde se kov elektrochemicky rozpouští.
Na méně aktivním povrchu, což je kladný pól mikroprvku (železo v páru Zn-Fe), jsou elektrony vázány v důsledku redukční reakce (katodový proces) podle schématu:
Přítomnost oxidačních činidel ve vodním filmu, která jsou schopna vázat elektrony, tedy umožňuje pokračovat v anodickém procesu. V souladu s tím se elektrochemická koroze může vyvinout pouze tehdy, pokud současně probíhají anodické i katodové procesy. V důsledku inhibice jednoho z nich se rychlost oxidace snižuje.

polarizační proces
Oba výše uvedené procesy způsobují polarizaci příslušných pólů (elektrod) mikroprvku. Jaké jsou zde vlastnosti? Obvykle je elektrochemická koroze kovů výrazněji zpomalena katodovou polarizací. Zvýší se tedy pod vlivem faktorů, které této reakci brání a jsou doprovázeny tzv. depolarizací kladné elektrody.
V mnoha korozních procesech se katodická depolarizace provádí vypouštěním vodíkových iontů nebo redukcí molekul vody a odpovídá vzorcům:
- V kyselém prostředí: 2H + + 2e \u003d H 2.
- V zásadě: 2H20 + 2e \u003d H2 + 2OH -.
Potenciální rozsah
Potenciál, který těmto procesům odpovídá, se v závislosti na charakteru agresivního prostředí může pohybovat od -0,83 do 0 V. Pro neutrální vodný roztok při teplotách blízkých normě je to přibližně -0,41 V. Proto vodíkové ionty, obsažené ve vodě a v neutrálních vodných systémech, mohou oxidovat pouze kovy s potenciálem menším než -0,41 V (nachází se v napěťové řadě až po kadmium). Vzhledem k tomu, že některé prvky jsou chráněny oxidovým filmem, je počet kovů vystavených oxidaci v neutrálním prostředí vodíkovými ionty nevýznamný.
Pokud mokrý film obsahuje rozpuštěný vzdušný kyslík, pak je schopen v závislosti na povaze prostředí vázat elektrony účinkem depolarizace kyslíku. V tomto případě je schéma elektrochemické koroze následující:
- O2 + 4e + 2H20 \u003d 4OH - nebo
- 02 + 4e + 4H+ = 2H20.
Potenciály těchto elektrodových reakcí při teplotách blízkých standardním kolísají od 0,4 V (alkalické) do 1,23 V (kyselé). V neutrálním prostředí odpovídá potenciál procesu redukce kyslíku za těchto podmínek hodnotě 0,8 V. To znamená, že rozpuštěný kyslík je schopen oxidovat kovy s potenciálem menším než 0,8 V (umístěné v sérii napětí až do stříbra ).

Nejdůležitější oxidační činidla
Typy elektrochemické koroze se vyznačují oxidačními prvky, z nichž nejvýznamnější jsou vodíkové ionty a kyslík. Film obsahující rozpuštěný kyslík je zároveň mnohem korozívnější než vlhkost, kde kyslík není, a který je schopen oxidovat kovy výhradně vodíkovými ionty, protože v druhém případě je počet typů materiálů schopných korodovat mnohem méně.
Například uhlíkové nečistoty jsou v oceli a litině přítomny především ve formě karbidu železa Fe 3 C. V tomto případě je mechanismus elektrochemické koroze s depolarizací vodíku u těchto kovů následující:
- (-) Fe-2e + nH20 = Fe2+ nH20 (může se tvořit rez);
- (+) 2H++ 2e \u003d H2 (v okyseleném prostředí);
- (+) 2H20 + 2e \u003d H2 + 2OH - (v neutrálním a alkalickém médiu).
Mechanismus koroze železa, které obsahuje příměsi mědi, v případě kyslíkové depolarizace katody popisují rovnice:
- (-) Fe-2e + nH20 = Fe2+ nH20;
- (+) 0,502 + H20 + 2e \u003d 2OH - (v okyseleném prostředí);
- (+) 0,502 + 2H + + 2e \u003d H20 (v neutrálním a alkalickém médiu).
Elektrochemická koroze probíhá různou rychlostí. Tento indikátor závisí na:
- potenciální rozdíl mezi póly galvanického mikroprvku;
- složení a vlastnosti elektrolytového prostředí (pH, přítomnost inhibitorů koroze a stimulantů);
- koncentrace (rychlost podávání) oxidačního činidla;
- teplota.
Metody ochrany
Elektrochemická ochrana kovů proti korozi se dosahuje následujícími způsoby:
- Výroba antikorozních slitin (legování).
- Zvýšení čistoty jednotlivých kovů.
- Nanášení různých ochranných nátěrů na povrch.
Tyto povlaky jsou zase:
- Nekovové (barvy, laky, maziva, emaily).
- Kovové (anodické a katodické povlaky).
- Vzniká speciální povrchovou úpravou (pasivace železa v koncentrované kyselině sírové nebo dusičné; železo, nikl, kobalt, hořčík v alkalických roztocích; tvorba oxidového filmu např. na hliníku).
Kovový ochranný povlak
Nejzajímavější a nejslibnější je elektrochemická ochrana proti korozi jiným druhem kovu. Podle charakteru ochranného účinku se metalizované povlaky dělí na anodické a katodické. Zastavme se u tohoto bodu podrobněji.
Anodový povlak je povlak tvořený aktivnějším (méně ušlechtilým) kovem, než je ten, který je chráněn. To znamená, že ochrana je prováděna prvkem, který je v sérii napětí až k základnímu materiálu (například potažení železa zinkem nebo kadmiem). Při lokální destrukci ochranné vrstvy bude méně ušlechtilý kovový povlak korodovat. V oblasti škrábanců a prasklin místní galvanický článek, katoda, ve které je chráněný kov, a anoda je povlak, který je oxidován. Na celistvosti takového ochranného filmu nezáleží. Čím je však tlustší, tím pomaleji se bude vyvíjet elektrochemická koroze a příznivý účinek bude trvat déle.
Katodický povlak je povlak s kovem s vysokým potenciálem, který je v sérii napětí po chráněném materiálu (např. nízkolegované oceli měď, cín, nikl, stříbro). Povlak musí být souvislý, protože při jeho poškození se tvoří lokální galvanické články, ve kterých bude základním kovem anoda a ochrannou vrstvou katoda.

Jak chránit kov před oxidací
Elektrochemická ochrana proti korozi se dělí na dva typy: obětní a katodickou. Ochranný povlak je podobný anodovému povlaku. K materiálu, který má být chráněn, je připevněna velká deska z aktivnější slitiny. Vznikne galvanický článek, ve kterém základní kov slouží jako katoda a chránič jako anoda (koroduje). Obvykle se pro tento typ ochrany používají slitiny na bázi zinku, hliníku nebo hořčíku. Chránič se postupně rozpouští, proto je nutné jej pravidelně vyměňovat.
Mnoho problémů ve veřejných službách a v průmyslu jako celku způsobuje elektrochemická koroze potrubí. V boji proti němu je nejvhodnější metoda katodické polarizace. K tomu se kovová struktura, která je chráněna před destruktivními oxidačními procesy, připojí k negativnímu pólu nějakého externího zdroje stejnosměrného proudu (z toho se pak stane katoda, zatímco rychlost vývoje vodíku se zvýší a rychlost koroze se sníží) a ke kladnému pólu je připojen kov nízké hodnoty.
Metody elektrochemické ochrany jsou účinné ve vodivém prostředí (příkladem je mořská voda). Proto se často používají chrániče k ochraně podvodních částí námořních plavidel.
Zpracování agresivního prostředí
Tato metoda je účinná, když k elektrochemické korozi železa dochází v malém objemu vodivé kapaliny. V tomto případě existují dva způsoby, jak se vypořádat s destruktivními procesy:
- Odstranění kyslíku z kapaliny (odvzdušnění) v důsledku proplachování inertním plynem.
- Zavádění inhibitorů do životního prostředí - tzv. inhibitory koroze. Například pokud dojde k destrukci povrchu v důsledku oxidace kyslíkem, přidávají se organické látky, jejichž molekuly obsahují určité aminokyseliny (imino-, thio- a další skupiny). Dobře se adsorbují na povrchu kovu a výrazně snižují rychlost elektrochemických reakcí vedoucích k destrukci povrchové kontaktní vrstvy.
Výstup
Chemická a elektrochemická koroze samozřejmě přináší značné škody jak v průmyslu, tak v běžném životě. Pokud by kov nekorodoval, výrazně by se zvýšila životnost mnoha předmětů, dílů, sestav, mechanismů. Nyní vědci aktivně vyvíjejí alternativní materiály, které mohou nahradit kov, které nejsou výkonově horší, ale je pravděpodobně nemožné úplně opustit jeho použití v krátkodobém horizontu. V tomto případě vystupují do popředí pokročilé metody ochrany kovových povrchů před korozí.