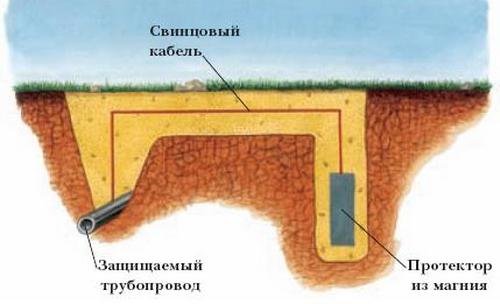
Схема за защитна защита срещу корозия. Преход в редица дизайни от метал. Отрицателен ефект от електрохимичната корозия
Електрохимична защита – ефективен методзащита на готовите продукти от електрохимична корозия. В някои случаи е невъзможно да се поднови боята или защитния опаковъчен материал, тогава е препоръчително да се използва електрохимична защита. Покритието на подземен тръбопровод или дъното на морски кораб е много трудоемко и скъпо за подновяване, понякога е просто невъзможно. Електрохимичната защита надеждно предпазва продукта от корозия, предотвратявайки разрушаването на подземни тръбопроводи, дъна на кораби, различни резервоари и др.
Поради фундаменталната важност на обсъждания проблем, започнаха изследвания върху ново поколение евтини устойчиви на хром покрития, които могат да се използват широко за защита срещу високотемпературна корозия. Иновативността на предложеното решение се проявява в покрития с ниска дебелина. Изследванията на окисление са проведени при постоянна температура, както и при условия на термичен удар.
Хромовите покрития се получават чрез магнетронно разпрашване. Установено е, че повърхностите на модифициращите клапани стават устойчиви на окисляване. Конференцията се проведе на английски езиксъс симултанен превод на целия курс на полски език.
Прилага се електрохимична защитав случаите, когато потенциалът за свободна корозия е в областта на интензивно разтваряне на основния метал или свръхпасивация. Тези. когато има интензивно разрушаване на металната конструкция.
Същността на електрохимичната защита
да приключи метален продуктпостоянен ток е свързан отвън (източник постоянен токили защитник). Електрическият ток върху повърхността на защитения продукт създава катодна поляризация на електродите на микрогалваничните двойки. Резултатът от това е, че анодните зони на металната повърхност стават катодни. И в резултат на излагане на корозивна среда не се разрушава металът на конструкцията, а анодът.
В него участваха повече от 150 художници и учени от 19 страни и присъстваха повече от 100 институции, от които над 80% са промишлени звена. Като започнем, ние се фокусираме основно върху техническите и финансовите аспекти на проекта. При извършване на антикорозионна защита екологични проблемиминимизиране на замърсяването по време на бластиране и нанасяне на боя. При антикорозионните работи това е много важно поради използването на материали, които са особено опасни за околната среда.
В зависимост от това в коя посока (положителна или отрицателна) се измества потенциалът на метала, електрохимичната защита се разделя на анодна и катодна.
Катодна защита от корозия
Катодна електрохимична защита от корозия се използва, когато защитеният метал не е склонен към пасивиране. Това е един от основните видове защита на металите от корозия. Същността на катодната защита е прилагането на външен ток от отрицателния полюс към продукта, който поляризира катодните участъци на корозионните елементи, приближавайки потенциалната стойност до анодните. Положителният полюс на източника на ток е свързан към анода. В този случай корозията на защитената конструкция е почти намалена до нула. Анодът постепенно се разрушава и трябва периодично да се сменя.
Въпреки това, не винаги знаем, че инвестирането може да бъде сериозна заплаха поради заобикалящата природа, особено поради околните птици. Инженерните конструкции са привлекателно място за създаване на нови местообитания на птици. Поради факта, че най-добрият период за извършване на антикорозионни работи в полето „съвпада“ с периода на земята на птиците, имаме работа с „конфликт на интереси“. Много често птиците, обитаващи инженерни обекти, принадлежат към защитени видове, което ще доведе до проблем. Изграждане на нови инженерни конструкцииИзграждането на нови инженерни конструкции е предприятие, което може да повлияе значително на околната среда и съгласно Закона за опазване на околната среда в такъв случай е необходимо получаване на т.нар. решения за условията на околната среда.
Има няколко варианта за катодна защита: поляризация от външен източник на електрически ток; намаляване на скоростта на катодния процес (например обезвъздушаване на електролита); контакт с метал, който има по-електроотрицателен потенциал за свободна корозия в дадена среда (т. нар. жертвена защита).
Задължението за получаване на това решение принадлежи на инвеститора и трябва да бъде получено преди вземането на други решения, необходими за инвестицията. Птиците са важен елемент от околната среда, която ни заобикаля, което налага това да се включи в екологично решение. Статията представя въздействието на битовите отпадъчни води върху бетонни пръстени, използвани за изграждане на помпени станции. Изпитванията са проведени върху проби от бетон и бетонови корозионни продукти, които са събрани от съществуващи и работещи канализационни кладенци.
Поляризацията от външен източник на електрически ток се използва много често за защита на конструкции, разположени в почвата, водата (дната на кораби и др.). Освен това този видАнтикорозионната защита се използва за цинк, калай, алуминий и неговите сплави, титан, мед и неговите сплави, олово, както и високохромни, въглеродни, легирани (както ниско, така и високолегирани) стомани.
Проблемът с разграждането на бетона засегна няколко кладенеца от цялата система за пречистване на отпадъчни води и в тази неизправна вентилация. Авторите посочват, че липсата на подходяща вентилация може да бъде потенциална причина микроклиматът да е силно агресивен към бетона. Проучването използва изследвания върху химическия анализ на бетона, както и микроскопски наблюдения. Освен това бяха проведени тестове за якост на бетона, за да се определят ефектите и степента на наблюдаваните промени, дължащи се на биологична корозия по отношение на промените в механичните свойства.
Външен източник на ток са станции за катодна защита, които се състоят от токоизправител (преобразувател), захранване на ток към защитената конструкция, анодни заземяващи електроди, еталонен електрод и аноден кабел.
катодна защитаприлага както самостоятелно, така и допълнителен изгледзащита от корозия.
Основният критерий, по който може да се прецени ефективността на катодната защита е защитен потенциал. Защитният потенциал е този, при който скоростта на корозия на метала в определени условиясреда приема най-ниската (доколкото е възможно) стойност.
Ключови думи: добре, сулфатна корозия, сулфатни бактерии. Покритията се характеризираха с изследване на тяхната морфология, химичен състав, дебелина и грапавост, както и устойчивостта на корозия на повърхностно модифицираната сплав. Доказано е положителното влияние на наличието на флуор в оксидния слой върху устойчивостта на корозия на пробите от сплав. Покритията са получени чрез химическо отлагане на пари с плазмен субстрат, създаден с помощта на радиочестотни електромагнитни вълни.
Трябва да се подчертае, че по-високите температури на двигателя и използването на алтернативни горива значително ускоряват разграждането на отделните компоненти на двигателя и особено на изпускателните клапани на двигателя. Добре известно е, че може да бъде податлив на проникване на хлорид. Процесът на хлориране е обект на много работи. Основната тема на тези изследвания е: корозията на стоманобетонната армировка и ефекта на хлоридите, химичното взаимодействие между клиони и циментовата матрица. Модификация чрез модификация чрез модификация направени от направени от направени от направени от направени от направени от направени от Ключови думи: физични свойства, бетон, варови материали, хлоридна среда, температура на околната среда.
Използването на катодна защита има недостатъци. Една от тях е опасност свръхзащита. Свръхзащитата се наблюдава при голямо изместване на потенциала на защитения обект в отрицателна посока. В същото време се откроява. В резултат на това разрушаването на защитните покрития, водородното крехкост на метала, корозионното напукване.
Известно е, че циментовият бетон може да бъде податлив на проникване на хлориди. Описанието на това явление за циментов бетон, произведен от нереактивна чакълна руда, вече е обект на многобройни работи. Работата взе предвид предимствата на метода и някои неудобства, които все още не са отстранени. Горните ефекти на корозия причиняват систематично намаляване на носещата способност на стоманобетонните елементи, така че оценката на армиращата корозия играе важна роля. След като се определи опасността от корозия на арматурата в тествания проект, трябва незабавно да вземете решение за специфичното отстраняване.
Защита на протектора (прилагане на протектора)
Един вид катодна защита е катодна защита. Използвайки защита на протекторакъм защитения обект се свързва метал с по-електроотрицателен потенциал. В този случай не се разрушава структурата, а протекторът. С течение на времето протекторът корозира и трябва да бъде заменен с нов.
В допълнение към визуалната оценка, напредъкът на процеса на корозия също беше количествено определен. Въведение Стоманата е важен конструктивен материал, приложим в много индустрии. Въпреки това, в много случаи е важно правилно да се предпазят стоманените повърхности на елементите от корозия. Един от начините за защита на стоманата от корозия е използването на метални покрития с аноден характер.
В случай на галванична клетка, това покритие е анод и претърпява разрушителни процеси на окисление; субстратът в тази система е катодът и не корозира. Някои от най-добрите анодни покрития включват електролитни цинкови покрития с метали от групата на желязото, т.е. никел, кобалт и желязо. Покритията от този тип се произвеждат електролитно. В индустрията често е необходимо да се маскират части от стоманени продукти чрез нанасяне на слой мед върху повърхността. След това този слой най-често се отстранява чрез ецване в разтвори на хромова киселина, което създава огромна опасност за околната среда.
Защитата на протектора е ефективна в случаите, когато има малко преходно съпротивление между протектора и околната среда.
Всеки протектор има свой защитен радиус, който се определя от максимума възможно разстояниевърху които протекторът може да бъде свален, без да се губи защитният ефект. Защитната защита се използва най-често, когато е невъзможно или трудно и скъпо да се подаде ток към конструкцията.
Работата анализира възможността за използване на разтвори, съдържащи водороден прекис като окислител и съединения, съдържащи медни комплекси. Въз основа на анализа на физикохимичните данни като потенциален комплекс е избрана етилендиаминтетраоцетна киселина. Експериментите показват, че разтворите, съдържащи това съединение, както и амоняк и водороден прекис, са идеални за ецване на мед от стоманена повърхност. Скоростта на ецване на медта в техния случай е няколко пъти по-висока, отколкото в случая на разтвори на хромова киселина, докато те не проявяват корозивна активност по отношение на стоманата.
Протекторите се използват за защита на конструкции в неутрална среда (морска или речна вода, въздух, почва и др.).
За производството на протектори се използват следните метали: магнезий, цинк, желязо, алуминий. Чистите метали не изпълняват в пълна степен своите защитни функции, поради което се легират допълнително при производството на протектори.
Тази обработка се използва за получаване на повърхностен слой с висока твърдост, като същевременно се поддържа здрава сърцевина. Най-често тези слоеве се отстраняват и след това се гравират в разтвори на хромова киселина, което причинява проблеми с околната среда. Възможност за замяна на разтвори на хромова киселина с проблеми с кислорода. Резултатите бяха допълнени от изследвания на микроструктурата на получените слоеве и измервания на грапавостта на повърхността. Получените резултати показват, че видът на процеса на нитрокарбонизация влияе върху микроструктурата и устойчивостта на корозия на получените повърхностни слоеве.
Железните протектори са изработени от въглеродни стоманиили чисто желязо.
Цинк протектори
Цинковите протектори съдържат около 0,001 - 0,005% олово, мед и желязо, 0,1 - 0,5% алуминий и 0,025 - 0,15% кадмий. Цинковите прожектори се използват за защита на продуктите от морска корозия (в солена вода). Ако цинковият протектор се използва в слабо солена, прясна вода или почва, той бързо се покрива с дебел слой оксиди и хидроксиди.
Ключови думи: нитроценови слоеве, титанови сплави, устойчивост на корозия, разтвор на Рингер Въведение Добро механични свойства, много добра устойчивост на корозия в много агресивни среди и биосъвместимост позволяват използването на титан и неговите сплави в множество медицински приложения.
Произвежда се основно от медицински инструменти и костни и сърдечни импланти, но поради наличието на ванадий в химията му, продължаващото му използване е под въпрос. Ванадий е широко признат като алергичен и канцерогенен елемент, който причинява възпаление. Обсъдени са методът и техниката за антикорозионна защита на стоманени елементи на хидравлични конструкции, експлоатирани в морска вода, особено в райони с променливи нива на водата и пръски. Въпросът се основава на защитата на купчина стоманени хидравлични конструкции на Северното пристанище в Гданск.
Протектор магнезий
Сплавите за производството на магнезиеви протектори са легирани с 2–5% цинк и 5–7% алуминий. Количеството мед, олово, желязо, силиций, никел в сплавта не трябва да надвишава десети и стотни от процента.
Магнезиевият протектор се използва в леко осолени, сладки води, почви. Протекторът се използва в среди, където цинковите и алуминиеви протектори са неефективни. Важен аспект е, че магнезиевите протектори трябва да се използват в среда с pH 9,5 - 10,5. Това се дължи на високата скорост на разтваряне на магнезия и образуването на слабо разтворими съединения на повърхността му.
Ключови думи: морски хидравлични съоръжения, корозия в зоната на различни водни нива и пръски, възстановяване на антикорозионната защита. Методология и спецификацииОписани са антикорозионна защита на водата, особено в районите на пълноводие и пръски. Пристанището се намира на северното пристанище в Гданск, Полша. Ключови думи: офшорни конструкции, корозия при прилив, обновяване на защитата от корозия Въведение Стоманените пилоти, използвани при изграждането на хидравлични конструкции в Северното пристанище в Гданск, са в експлоатация от половин век.
Магнезиевият протектор е опасен, т.к. е причина за водородно крехкост и корозионно напукване на конструкциите.
Алуминиеви протектори
Алуминиеви протектори съдържат добавки, които предотвратяват образуването на алуминиеви оксиди. В такива протектори се въвеждат до 8% цинк, до 5% магнезий и десети до стотни силиций, кадмий, индий и талий. Алуминиеви протектори се използват в крайбрежния шелф и течаща морска вода.
Трябва да се подчертае, че антикорозионната защита от самото начало на тази купчина е възникнала само върху част от повърхността под формата на битумно покритие от стоманени тръбни пилоти. Представен е проблемът с дефектността на антикорозионната защита в областта на боядисването на защитно-декоративни покрития върху стоманени елементи на прегради, предварително защитени чрез горещо поцинковане. Използвайки примери от различни сайтове, проблемът с разслояването на бояджийски покрития се повтаря, независимо от вида на използваните бои и значителното развитие на корозия върху открит цинков субстрат.
Анодна защита от корозия
Анодна електрохимична защита се използва за конструкции от титан, нисколегирани неръждаеми, въглеродни стомани, високолегирани черни сплави, различни пасивирани метали. Анодната защита се използва в силно проводими корозивни среди.
Обърнато е внимание и на случаи на нарушения, свързани със същите елементи, но свързани с липсата на надлежен надзор при изпълнение на антикорозионните работи. Ключови думи: прахова боя, полиестерна прахова боя, мостов обект, мостозащитна бариера, боядисване върху поцинкована стомана, дуплексна защита, дефекти на боядисаното покритие, грешки при изпълнение на елементите, направени на базата на горещо поцинковане. Примери, взети от различни покрития.
Разпознаване на проблеми с повърхността на боята. Внимание важи и за други случаи на повреда. Ключови думи: мостови бои, полиестерни покрития, мостове, покрития, мостове, бояджийски покрития върху поцинкована стомана, защитни покрития върху мостови конструкции. Основният елемент на повечето мостови конструкции са различни видове защитни бариери.
При анодна защита потенциалът на защитения метал се измества към по-положителна страна, докато се достигне пасивно стабилно състояние на системата. Предимствата на анодната електрохимична защита са не само много значително забавяне на скоростта на корозия, но и факта, че корозионните продукти не влизат в продукта и средата.
Анодната защита може да бъде реализирана по няколко начина: чрез изместване на потенциала към положителната страна с помощта на външен източник на електрически ток или чрез въвеждане на окислители (или елементи в сплавта) в корозивната среда, които повишават ефективността на катодния процес върху метална повърхност.
Анодната защита с използването на окислители е подобна по своя защитен механизъм на анодната поляризация.
Ако се използват пасивиращи инхибитори с окислителни свойства, тогава защитената повърхност преминава в пасивно състояние под действието на възникналия ток. Те включват дихромати, нитрати и др. Но те замърсяват доста силно заобикалящата технологична среда.
С въвеждането на добавки в сплавта (главно легиране с благороден метал), реакцията на редукция на деполяризаторите, протичаща при катода, протича с по-ниско пренапрежение, отколкото върху защитения метал.
Ако минем през защитената конструкция електричество, потенциалът се измества в положителна посока.
Инсталацията за анодна електрохимична защита от корозия се състои от външен източник на ток, референтен електрод, катод и самия защитен обект.
За да се установи дали е възможно да се приложи анодна електрохимична защита за определен обект, се вземат анодни поляризационни криви, с помощта на които е възможно да се определи корозионният потенциал на изследваната конструкция в определена корозивна среда, област на стабилна пасивност и плътност на тока в тази област.
За производството на катоди се използват нискоразтворими метали, като високолегирани неръждаеми стомани, тантал, никел, олово и платина.
За да бъде ефективна анодната електрохимична защита в определена среда, е необходимо да се използват лесно пасивирани метали и сплави, референтният електрод и катодът трябва винаги да са в разтвор, а свързващите елементи да са с високо качество.
За всеки случай на анодна защита, разположението на катодите е проектирано индивидуално.
За да анодна защитае бил ефективен за определен обект, необходимо е той да отговаря на някои изисквания:
Всичко заваркитрябва да бъде с високо качество;
В технологичната среда материалът, от който е изработен защитеният обект, трябва да премине в пасивно състояние;
Броят на въздушните джобове и слотове трябва да бъде сведен до минимум;
Върху конструкцията не трябва да има нитови съединения;
В устройството, което трябва да бъде защитено, референтният електрод и катодът трябва винаги да са в разтвор.
За прилагане на анодна защита в химическата промишленост често се използват топлообменници и цилиндрични възли.
Електрохимична анодна защита неръждаеми стоманиприложим за промишлени складове на сярна киселина, разтвори на базата на амоняк, минерални торове, както и всички видове колектори, резервоари, измервателни резервоари.
Анодната защита може да се използва и за предотвратяване на повреди от корозия в вани за химическо никелиране, топлообменници при производството на изкуствени влакна и сярна киселина.
Корозията е процес на спонтанно разрушаване на повърхността на материалите поради взаимодействие с околната среда. Причината му е термодинамична нестабилност. химични елементикъм определени вещества. Формално полимерите, дървото, керамиката, каучукът са подложени на корозия, но терминът „стареене“ се използва по-често за тях. Най-сериозни щети причинява ръждясването на металите, за защита на които се разработват високотехнологични противодействие. Но за това ще говорим по-късно. Учените правят разлика между химическа и електрохимична корозия на металите.
Химическа корозия
Обикновено се появява, когато метална конструкция е изложена на сухи газове, течности или разтвори, които не провеждат електрически ток. Същността на този вид корозия е прякото взаимодействие на метала с агресивна среда. Елементите химически корозират по време на топлинна обработка или в резултат на дългосрочна експлоатацияпри достатъчно високи температури. Това се отнася за лопатки на газови турбини, фитинги за топилни пещи, части от двигатели с вътрешно горене и т.н. В резултат на това на повърхността се образуват определени съединения: оксиди, нитриди, сулфиди.
Това е следствие от контакта на метал с течна среда, способна да провежда електрически ток. Поради окисляването материалът претърпява структурни промени, водещи до образуване на ръжда (неразтворим продукт), или металните частици преминават в разтвор на йони.
Електрохимична корозия: примери
Разделя се на:
- Атмосферно, което възниква, когато върху повърхността на метала има течен филм, в който газовете, съдържащи се в атмосферата (например O 2, CO 2, SO 2), са в състояние да се разтворят с образуването на електролитни системи.
- Течност, която тече в проводяща течна среда.
- Подземни води, които текат под въздействието на подземните води.

Причини
Тъй като обикновено всеки метал, който се използва за промишлени нужди, не е идеално чист и съдържа включвания от различно естество, електрохимичната корозия на металите възниква поради образуването на голям брой локални галванични клетки с късо съединение върху повърхността на желязото.
Появата им може да бъде свързана не само с наличието на различни (особено метални) примеси (контактна корозия), но и с хетерогенност на повърхността, дефекти на кристалната решетка, механични повреди и други подобни.
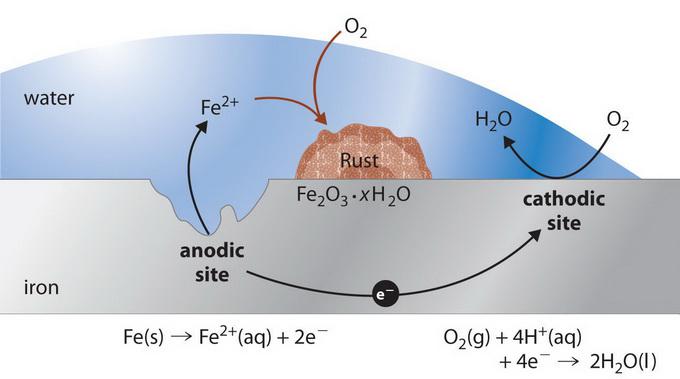
Механизъм на взаимодействие
Процесът на електрохимична корозия зависи от химичния състав на материалите и характеристиките на външната среда. Ако така нареченият технически метал е покрит с мокър филм, тогава във всеки от тези галванични микроелементи, които се образуват на повърхността, протичат две независими реакции. По-активният компонент на корозионната двойка дарява електрони (например цинк в двойка Zn-Fe) и преминава в течната среда като хидратирани йони (тоест корозира) съгласно следната реакция (аноден процес):
M + nH 2 O \u003d M z + * nH 2 O + ze.
Тази част от повърхността е отрицателният полюс на локалния микроелемент, където металът се разтваря електрохимично.
Върху по-малко активната част на повърхността, която е положителният полюс на микроелемента (желязо в двойка Zn-Fe), електроните се свързват поради редукционната реакция (катоден процес) по схемата:
По този начин, наличието на окислители във водния филм, които са способни да свързват електрони, прави възможно продължаването на анодния процес. Съответно, електрохимичната корозия може да се развие само ако анодните и катодни процеси протичат едновременно. Поради инхибирането на един от тях, скоростта на окисляване намалява.

процес на поляризация
И двата горни процеса предизвикват поляризация на съответните полюси (електроди) на микроелемента. Какви са характеристиките тук? Обикновено електрохимичната корозия на металите се забавя по-значително от катодната поляризация. Следователно, той ще се увеличи под въздействието на фактори, които предотвратяват тази реакция и са придружени от така наречената деполяризация на положителния електрод.
При много процеси на корозия катодната деполяризация се осъществява чрез изхвърляне на водородни йони или чрез редукция на водни молекули и съответства на формулите:
- В кисела среда: 2H + + 2e \u003d H 2.
- В алкални: 2H 2 O + 2e \u003d H 2 + 2OH -.
Потенциален обхват
Потенциалът, който съответства на тези процеси, в зависимост от естеството на агресивната среда, може да варира от -0,83 до 0 V. За неутрален воден разтвор при температури, близки до стандартните, той е приблизително -0,41 V. Следователно, водородните йони, съдържащи се във вода и в неутрални водни системи, могат да окисляват само метали с потенциал по-малък от -0,41 V (разположен в серия на напрежение до кадмий). Като се има предвид, че някои от елементите са защитени с оксиден филм, броят на металите, подложени на окисляване в неутрални среди от водородни йони, е незначителен.
Ако мокрият филм съдържа разтворен кислород във въздуха, тогава той е способен, в зависимост от естеството на средата, да свързва електрони чрез ефекта на кислородна деполяризация. В този случай схемата на електрохимичната корозия е, както следва:
- O 2 + 4e + 2H 2 O \u003d 4OH - или
- O 2 + 4e + 4H + = 2H 2O.
Потенциалите на тези електродни реакции при температури, близки до стандартните, варират от 0,4 V (алкални) до 1,23 V (киселинни). В неутрална среда потенциалът на процеса на редукция на кислород при тези условия съответства на стойност от 0,8 V. Това означава, че разтвореният кислород е в състояние да окислява метали с потенциал под 0,8 V (разположен в серия от напрежения до сребро ).

Най-важните окислители
Видовете електрохимична корозия се характеризират с окислителни елементи, най-важните от които са водородни йони и кислород. В същото време филмът, съдържащ разтворен кислород, е много по-корозивен от влагата, където няма кислород и който е способен да окислява металите изключително с водородни йони, тъй като в последния случай броят на видовете материали, способни да корозират, е много по-малко.
Например въглеродните примеси присъстват в стоманата и чугуна главно под формата на железен карбид Fe 3 C. В този случай механизмът на електрохимична корозия с водородна деполяризация за тези метали е както следва:
- (-) Fe - 2e + nH 2 O = Fe 2+ nH 2 O (може да се образува ръжда);
- (+) 2H + + 2e \u003d H 2 (в подкиселена среда);
- (+) 2H 2 O + 2e \u003d H 2 + 2OH - (в неутрална и алкална среда).
Механизмът на корозия на желязото, което съдържа медни примеси, в случай на кислородна деполяризация на катода се описва с уравненията:
- (-) Fe - 2e + nH2O = Fe2+ nH2O;
- (+) 0,5O 2 + H 2 O + 2e \u003d 2OH - (в подкиселена среда);
- (+) 0,5O 2 + 2H + + 2e \u003d H 2 O (в неутрална и алкална среда).
Електрохимичната корозия протича с различна скорост. Този индикатор зависи от:
- потенциална разлика между полюсите на галваничен микроелемент;
- съставът и свойствата на електролитната среда (рН, наличието на инхибитори на корозия и стимуланти);
- концентрация (скорост на подаване) на окислителя;
- температура.
Методи за защита
Електрохимичната защита на металите от корозия се постига по следните начини:
- Създаване на антикорозионни сплави (легиране).
- Повишаване чистотата на отделния метал.
- Нанасяне на различни защитни покрития върху повърхността.
Тези покрития от своя страна са:
- Неметални (бои, лакове, лубриканти, емайли).
- Метални (анодни и катодни покрития).
- Образува се чрез специална повърхностна обработка (пасивиране на желязо в концентрирана сярна или азотна киселина; желязо, никел, кобалт, магнезий в алкални разтвори; образуване на оксиден филм, например върху алуминий).
Метално защитно покритие
Най-интересна и обещаваща е електрохимичната защита срещу корозия от друг вид метал. Според естеството на защитния ефект метализираните покрития се делят на анодни и катодни. Нека се спрем на този момент по-подробно.
Анодното покритие е покритие, образувано от по-активен (по-малко благороден) метал от този, който е защитен. Тоест, защитата се осъществява от елемент, който е в серия от напрежения до основния материал (например покритие на желязото с цинк или кадмий). При локално разрушаване на защитния слой по-малко благородното метално покритие ще корозира. В областта на драскотини и пукнатини, местен галванична клетка, катодът в който е защитеният метал, а анодът е покритието, което се окислява. Целостта на такъв защитен филм няма значение. Колкото по-дебел е обаче, толкова по-бавно ще се развие електрохимична корозия и полезният ефект ще продължи по-дълго.
Катодно покритие е покритие с метал с висок потенциал, който в поредица от напрежения е след защитения материал (например разпръскване нисколегирани стоманимед, калай, никел, сребро). Покритието трябва да бъде непрекъснато, тъй като ако е повредено, се образуват локални галванични клетки, в които основният метал ще бъде анод, а защитният слой ще бъде катодът.

Как да предпазим метала от окисляване
Електрохимичната защита от корозия е разделена на два вида: жертвена и катодна. Защитното покритие е подобно на анодното покритие. Голяма плоча от по-активна сплав е прикрепена към материала, който трябва да бъде защитен. Образува се галванична клетка, в която основният метал служи като катод, а протекторът служи като анод (корозира). Обикновено за този вид защита се използват сплави на основата на цинк, алуминий или магнезий. Протекторът постепенно се разтваря, така че трябва периодично да се сменя.
Много проблеми в комуналните услуги и в индустрията като цяло са причинени от електрохимичната корозия на тръбопроводите. В борбата с него най-подходящ е методът на катодната поляризация. За да направите това, метална конструкция, която е защитена от разрушителни процеси на окисление, се свързва към отрицателния полюс на някакъв външен източник на постоянен ток (след това става катод, докато скоростта на отделяне на водород се увеличава и скоростта на корозия намалява), и към положителния полюс е прикрепен метал с ниска стойност.
Методите за електрохимична защита са ефективни в проводяща среда (морската вода е отличен пример). Ето защо, протекторите често се използват за защита на подводните части на морските съдове.
Обработка на агресивна среда
Този метод е ефективен, когато електрохимичната корозия на желязото настъпва в малък обем проводяща течност. В този случай има два начина за справяне с деструктивните процеси:
- Отстраняване на кислород от течността (обезвъздушаване) в резултат на продухване с инертен газ.
- Въвеждането на инхибитори в околната среда - така наречените инхибитори на корозия. Например, ако повърхността се разруши в резултат на окисление с кислород, се добавят органични вещества, чиито молекули съдържат определени аминокиселини (имино-, тио- и други групи). Те са добре адсорбирани върху металната повърхност и значително намаляват скоростта на електрохимичните реакции, водещи до разрушаване на повърхностния контактен слой.
Изход
Разбира се, химическата и електрохимичната корозия нанася значителни щети както в индустрията, така и в ежедневието. Ако металът не корозира, експлоатационният живот на много елементи, части, възли, механизми ще се увеличи значително. Сега учените активно разработват алтернативни материали, които могат да заменят метала, които не са по-ниски по отношение на производителността, но вероятно е невъзможно напълно да се откаже от употребата му в краткосрочен план. В този случай на преден план излизат модерните методи за защита на металните повърхности от корозия.