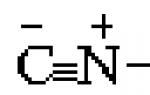Chemici z Moskevské státní univerzity vytvořili protijed na nejsilnější chemické zbraně. Chemici z Moskevské státní univerzity vytvořili protijed na nejsilnější chemické zbraně.Látky zkoumali dva vědci
Ruští vědci zkoumali částice meteoritové hmoty a dospěli k závěru, že mikroorganismy, které přišly na Zemi z vesmíru, jsou o jeden a půl miliardy let starší než pozemské formy života. To znamená, že život na Zemi mohl vzniknout mnohem později než na jiných planetách.
Každý den spadne na naši planetu z vesmíru 100 až 1000 tun mimozemské hmoty – ve formě prachu a meteoritů. Specialisté z Paleontologického ústavu Ruské akademie věd, kteří studovali strukturu vesmírných poslů, v nich našli to, co ve skutečnosti celé lidstvo dlouho doufalo, že najde ve vesmíru - stopy života!
Lidstvo se vždy zajímalo o to, co se děje mimo Zemi, a jedna z hlavních otázek, která nás pronásleduje, je: existuje nebo byl život daleko od naší planety? Otázka existence mimozemského života byla opakovaně vznesena vědci z různých zemí. Nové kolo výzkumných aktivit v tomto směru začalo v roce 1996, kdy skupina amerických vědců vedená Davidem McKayem publikovala článek, ve kterém bylo navrženo, že uvnitř některých meteoritů jsou stopy fosilních bakterií, pravděpodobně marťanského původu. Z této práce vyplynulo, že pokud na Marsu nyní není žádný život, pak tam kdysi dávno ve vzdálených dobách mohl být na primitivní úrovni.
Od vydání McKayovy publikace výzkumníci nashromáždili obrovské množství nového materiálu na toto téma. Například do konce letošního roku se specialisté z Paleontologického ústavu Ruské akademie věd spolu s kolegy z NASA chystají vydat „Atlas biomorfních struktur“, který shrne všechny informace posledních let. Publikace je plánována na dvě části. První se zaměří na organické zbytky v zemských horninách a druhý na biomorfní struktury v meteoritech. Alexey Rozanov, ředitel Paleontologického institutu Ruské akademie věd, doktor geologických a mineralogických věd, řekl Itogimu o tom, jaké neobvyklé věci se jim podařilo vidět ve struktuře meteoritů.
Prostorové parcely
Všechny meteority, které dopadly na Zemi, lze podle složení rozdělit na kamenné, železné a železné. Vědci nacházejí zbytky biomorfních struktur pouze v jedné z odrůd kamenných meteoritů - uhlíkatých chondritech (tento název dostali podle chondrul přítomných v jejich struktuře - kulovité silikátové útvary). Řešení problému původu uhlíkatého materiálu v takových meteoritech je zásadně důležité, protože na něm závisí vývoj představ o původu života obecně a na Zemi zvláště. A proto není divu, že hlavními objekty pro vědeckou práci byly kamenné meteority tohoto typu - Efremovka (nalezena v Kazachstánu v roce 1962) a Murchison (Austrálie, 1969). Pomocí elektronického mikroanalyzátoru odborníci zkoumali složení minerální matrice prvního a poté druhého meteoritu. A objevili následující: v obou případech byly uvnitř matrice fosilní částice vláknitých mikroorganismů, připomínající nižší houby, které si zachovaly detaily buněčné struktury, a také (a to je nejdůležitější!) zkamenělé zbytky určité bakterie.
Bylo možné porovnat biomorfní struktury nalezené v meteoritech s moderními mikroorganismy, stejně jako se vzorky bakteriálního světa starověku. Tyto experimenty položily základ pro nový směr ve vědě – „bakteriální paleontologii“. Jak říkají sami paleontologové, jde o další klíč k rozluštění kosmického organického materiálu. Moderní pozemské analogy mikroorganismů nalezených v meteoritech se ukázaly být modrozelené řasy nebo sinice.
Pro informaci: sinice jsou nejstarší fotosyntetické organismy, jejichž životně důležitá aktivita, jak věda s jistotou ví, zbavila starodávnou atmosféru Země oxidu uhličitého a poskytla jí kyslík. Právě sinice se spolu se svými doprovodnými bakteriemi staly na více než tři miliardy let úplnými vládci Země a do značné míry určovaly průběh tak významných geologických událostí, jako je nahromadění mnoha usazených hornin a minerálů. Společenstva vytvořené těmito mikroorganismy, které mají úzké metabolické vazby, se v průběhu historie Země ukázaly jako překvapivě stabilní. Pravda, více organizovaní konkurenti je postupně vytlačili z širých mořských oblastí do ekologických nik, hlavně s extrémními podmínkami, jako jsou hypersolné laguny a vulkanické oblasti. A v těchto místech mikrobiální společenstva přetrvávají dodnes.
Přítomnost analogů sinic v uhlíkaté hmotě meteoritů tak přiměla vědeckou komunitu uznat nepochybný fakt jejich biogenního původu. Co to dokazuje? Skutečnost, že významná morfologická jednota pozemských mikrobiálních organismů, moderních i starověkých, s formacemi v meteoritech, dává důvod hovořit o základní jednotě mikrobiologického světa Země a dalších vesmírných objektů.
Pozůstatky mikroorganismů, pravděpodobně patřících sinicím, mohou naznačovat i senzační fakt, že ke vzniku uhlíkatých chondritů došlo ve vodním prostředí. Z toho nevyhnutelně vyplývá, že minimálně před 4,5-4,6 miliardami let existoval někde za Zemí život, alespoň na úrovni bakterií a možná i nižších hub. Tento věk je srovnatelný s dobou počátku formování Země. Na tomto základě paleontologové usoudili, že někde ve vesmíru se bakteriální svět objevil dříve než na naší planetě. A kdo by popřel, že se mohl dále vyvíjet zcela jinou, nadpozemskou cestou? Možná se někde na vzdálených planetách vytvořily formy života, které se zásadně liší od těch pozemských a o kterých moderní věda nemá nejmenší tušení. Někdo to bude nazývat sci-fi, ale jak si člověk nemůže vzpomenout, že až donedávna byla možnost přítomnosti vody na Marsu považována za absurdní.
„Objev mikroorganismů v kamenných meteoritech nás nutí výrazně přehodnotit mnohé zavedené představy o vývoji sluneční soustavy a původu života,“ říká Alexey Rozanov, „A ještě jeden důležitý bod: věk mikroorganismů nám dává příležitost bojovat proti mylné představě, že vesmírná tělesa jsou přenašeči nebezpečných bakterií."Zkamenělé mikroby, které přicházejí na Zemi v meteoritech, jsou neškodné. Koneckonců jsou mrtvé několik miliard let."
Další etapa fascinujícího výzkumu souvisela se studiem procesu fosilizace mikroorganismů. A zde se také vědci setkali s nečekanými výsledky. „Výsledek laboratorních experimentů byl ohromující," říká Alexey Rozanov. „Ukázalo se, že proces fosilizace může trvat jen několik hodin. Dříve jsme předpokládali, že všechny fosilní organismy zkameněly téměř miliony let. Ukázalo se však, že toto není vůbec povinným požadavkem. Vysoká Rychlost tohoto procesu vysvětluje, proč jsou bakterie, které nacházíme ve starých kamenech, tak dobře zachovány.“
Dalším důkazem toho, že v meteoritech spadlých na Zemi jsou bakterie a ne něco jiného, byl objev magnetitových krystalů a kulovitých těles složených z malých krystalů (framboidů) v nich. Faktem je, že na Zemi se takové bizarní struktury tvoří pouze za přímé účasti mikroorganismů.
Navzdory tomu, že paleontologický výzkum v tomto směru postupuje poměrně rychle, stále se na cestě objevují určité potíže. Vyjadřují se například názory, že je stěží možné hovořit o čistotě experimentů, protože meteority mohou být „kontaminovány“ pozemskými mikroorganismy. Odborníci z Paleontologického ústavu se shodují, že kosmická tělesa jsou po dosažení naší planety vystavena pronikání mikroorganismů do nich, ale tento problém nepovažují za neřešitelný. Vědci, kteří přibližně znají složení meteoritové hmoty, se naučili určit, do jaké míry si pozemské mikroorganismy osvojily vesmírné artefakty. Pokud množství jakékoli složky v meteoritu přesahuje její možný obsah, znamená to, že je beznadějně „ucpaný“.
„Během našeho výzkumu jsme analyzovali téměř dva tucty meteoritů a téměř ve všech případech byly nalezeny staré zkameněliny,“ říká Alexey Rozanov. zemské horniny. Na základě těchto studií můžeme s jistotou říci, že mikroorganismy v meteoritech jsou prastaré bakterie. Rozmanitost nalezených organismů může také naznačovat různá prostředí pro tvorbu mikrobiálních společenstev, od termálních po jezerní. Zároveň samozřejmě, my Nevylučujeme možnost objevit v budoucnu takové formy, které nebudou mít pozemské obdoby."
Těžko uvěřit
Závěry Alexeje Rozanova jsou velmi neobvyklé, a proto jsou ve vědecké komunitě přijímány nejednoznačně. „Itogi“ to mohl ověřit rozhovorem s hlavními odpůrci uznávaného vědce. Například vedoucí laboratoře meteoritiky na Ústavu geochemie a analytické chemie pojmenované po. V.I. Vernadsky RAS, doktor geologických a mineralogických věd Michail Nazarov pevně věří, že dnes neexistují žádná spolehlivá fakta, která by naznačovala možnost přítomnosti zbytků organické hmoty v meteoritech: „Tento problém byl studován opakovaně a existují lidé, kteří věří do toho. Například Alexey Yuryevich Rozanov. Věří, že našel nějaké zbytky mikroorganismů. Ale nemyslím si, že tato věc byla stoprocentně prokázána."
A zde je názor Alexandra Uljanova, doktora geologických a mineralogických věd, profesora katedry mineralogie Moskevské státní univerzity, člena Výboru pro meteority Ruské akademie věd: „Rozanovův pohled je mi znám. Četl jsem jeho vědecké publikace, ale v mnoha ohledech s ním nesouhlasím.Začněme tím, že Alexey Yuryevich studoval uhlíkatého chondrita Efremovka, ve kterém údajně našel organické látky - něco, co připomíná zkamenělé bakterie.Ale zároveň čas ležel tento meteorit na polích, která byla oplodněna různými aktivními složkami asi čtyřicet let. Zejména podél puklin uvnitř meteoritu "je patrná oxidace železem. Proto tento nález nepovažuji za spolehlivý. Ale je to pouze můj pohled. Navíc nevěřím v objevy mikroorganismů uvnitř marťanských meteoritů a považuji taková tvrzení za nespolehlivá a nepodložená."
Přišly starověké bakterie z vesmíru nebo pocházejí ze Země? Odpověď na tuto otázku dostaneme až poté, co vědecký výzkum dospěje ke svému závěru. Již dnes je však jasné, že nové způsoby hledání života ve Vesmíru nutí vědu přehodnotit zavedené představy o vývoji a původu Sluneční soustavy.
Jekatěrina Gorbunová
POZADÍ
Kontroverzní věda
15. března 1806 spadl kamenný meteorit ve městě Alais (Francie). Byl to první uhlíkatý chondrit, který byl intenzivně studován. Takže v roce 1834 byl švédský chemik Berzelius, který studoval jeho vzorek, překvapen, když v něm objevil vodu, a také si všiml podobnosti uhlíkaté látky meteoritu s pozemským biologickým materiálem.
Dne 14. května 1864 spadlo u francouzských vesnic Noïc a Orgueil více než 20 černých kamenů (některé o váze asi 2 kg). Bezprostředně po pádu vesničané posbírali modročerné skály, z nichž mnohé byly zcela zakryté. Meteorit Orgay byl okamžitě podroben důkladné chemické a mineralogické analýze. Obsah uhlíku v jeho úlomcích byl tak vysoký, že tato skutečnost byla zpočátku považována za důsledek kontaminace pozemskou hmotou. Později se však dospělo k závěru, že na vzniku meteoritu se velmi pravděpodobně podílel živý materiál.
Hypotéza o existenci mimozemských „životu podobných“ forem v meteoritech, poprvé předložená v polovině 19. století, byla poměrně široce přijímána a úspěšně existovala téměř jedno století – až do 60. let 20. století. V roce 1962 se američtí výzkumníci Anders a Fitch postavili proti biogenní povaze meteoritového materiálu a uvedli, že fosilie v nich nemají analogy, a proto by měla být biogenní povaha odmítnuta. Předpokládali, že předpokládané mikroorganismy nejsou biologickými objekty, a všechna ostatní biologicky podobná tělesa považovali za pozemské znečištění – „muzeální prach“ a „pyl“. Anders a Fitch jsou stále považováni za nejaktivnější kritiky verze o přítomnosti mikroorganismů v meteoritech.
V roce 1964 sovětský vědec Boris Timofeev publikoval v Německu článek o objevu útvarů připomínajících fytoplankton pozemského typu v meteoritu Migey. Článek byl roztrhán na kusy. Mimochodem, mezi kritiky byl Alexey Rozanov, který dnes podle něj změnil svůj pohled na tuto publikaci.
V roce 1966 nositel Nobelovy ceny za chemii G. K. Urey zhodnotil důkazy o biologických materiálech v meteoritech. Poznamenal, že v meteoritech jsou organické látky, které se velmi podobají těm ze starověkých pozemských hornin, že organické látky nalezené v uhlíkatých chondritech se nepodobají těm, které jsou přítomné v moderním znečištění. Urey poznamenal: "... některé látky v meteoritech, pokud by byly nalezeny v pozemských objektech, by byly nepochybně považovány za biogenní."
Otázka: Dva vědci zkoumali látky získané v jejich laboratořích. Jeden pomocí fyzikálních metod zjistil, že molekula jeho látky A obsahuje 2 atomy uhlíku, šest atomů vodíku a jeden atom kyslíku. Další pomocí chemických metod zjistil, že 5 gramů její látky B obsahuje 2,61 g uhlíku, 0,652 g vodíku a také kyslík. Stanovením molekulové hmotnosti látky získal stejnou hodnotu jako první vědec. V korespondenci se dohodli na výpočtu a srovnání hmotnostních zlomků prvků v jejich sloučeninách. Druhý vědec také slíbil, že stanoví vzorec své látky. Pokuste se provést výpočty, které tito vědci museli udělat. Stačí získaná data k tomu, aby bylo možné říci, že studovali stejnou látku?
Dva vědci zkoumali látky získané v jejich laboratořích. Jeden pomocí fyzikálních metod zjistil, že molekula jeho látky A obsahuje 2 atomy uhlíku, šest atomů vodíku a jeden atom kyslíku. Další pomocí chemických metod zjistil, že 5 gramů její látky B obsahuje 2,61 g uhlíku, 0,652 g vodíku a také kyslík. Stanovením molekulové hmotnosti látky získal stejnou hodnotu jako první vědec. V korespondenci se dohodli na výpočtu a srovnání hmotnostních zlomků prvků v jejich sloučeninách. Druhý vědec také slíbil, že stanoví vzorec své látky. Pokuste se provést výpočty, které tito vědci museli udělat. Stačí získaná data k tomu, aby bylo možné říci, že studovali stejnou látku?
Odpovědi:
Podobné otázky
- Lyuba dal do košíku 2 svazky mrkví, každý po 7. Kolik mrkví je v košíku?
- 6. třída, potřebuji čísla 4 a 5, předem děkuji)
- Skicák je 8x dražší než tužka, ale dohromady stojí 135 rublů Kolik stojí album?
- Dva paprsky BD a BK jsou vytaženy z vrcholu rozvinutého úhlu ABC tak, že úhel ABK = 128° úhel CBD = 164° Vypočítejte hodnotu úhlu DBK
- Které z následujících je fyzické tělo? kapka vodní můra ocel východ slunce. 2K? Které z fyzických těles nelze spojit kompresí? 3 kusy plastelíny, kusy litiny, skleněné úlomky, kapky vody. 3
V historii chemie byly časté případy, kdy k otravě, poranění nebo dokonce smrti nedošlo v důsledku dlouhodobé práce s toxickými látkami, ale v důsledku jedné neúspěšné zkušenosti, obvykle doprovázené výbuchem. Níže je zdaleka ne úplný seznam takových incidentů.
A Při studiu vlastností jím objevené látky, které se později říkalo Bertholletova sůl, francouzský chemik C. L. Berthollet (1748–1822) málem zemřel.
Při jednom z pokusů získat draslík zahříváním směsi hydroxidu draselného s práškovým železem málem přišli o život francouzští vědci J. L. Gay-Lussac (1778–1850) a L. J. Thénard (1777–1857). Aby se Gay-Lussac zotavil ze svých ran, musel strávit téměř měsíc a půl v posteli a jeho zrak dočasně zmizel. Tenar málem zemřel ještě jednou v chemické laboratoři. V roce 1825 na přednášce, chtěje uhasit žízeň, omylem vypil tekutinu ze sklenice, která obsahovala roztok sublimátu (sublimát HgCl 2 je znám jako silný jed). Život mu zachránil pouze včasný protijed v podobě syrových vajec.
Obětí další nehody se stal francouzský chemik a fyzik Pierre-Louis Dulong (1785–1838). V roce 1811, při studiu chloridu dusnatého, došlo v jeho laboratoři k explozi, která vědce těžce otřesila. Navzdory tomu se Dulong rozhodl ve výzkumu látky pokračovat. V říjnu 1812 ho nový výbuch připravil o oko a znetvořil ruku. Dulongovo druhé oko bylo také poškozeno. Vědci bylo v té době pouhých 27 let.
Velký švédský chemik J. J. Berzelius (1779–1848) se na jaře roku 1818 při práci se selenovodíkem vážně otrávil.
V rukou německého chemika R. W. Bunsena (1811–1899) 9. listopadu 1836 explodovala zapečetěná skleněná nádoba obsahující sloučeninu arsenu, což vedlo málem ke smrti vědce. Úlomek skla zasáhl Bunsenovo pravé oko a navždy ho oslepil. Vědec byl navíc otráven.
K silnému výbuchu došlo také u francouzského chemika S.A.Wurtze (1817–1884), když v otevřené zkumavce zahříval směs chloridu fosforitého a sodíku. Četné úlomky vážně poranily vědcovu tvář a ruce. Sklo se mi dostalo do očí. Úlomky nebylo možné okamžitě odstranit. Teprve postupem času začaly postupně mizet a chirurgové museli využít všech svých schopností, aby zachovali Wurtzův zrak.
Život budoucího nositele Nobelovy ceny, německého organického chemika A. Bayera (1835–1917), mohl v mládí skončit tragicky. Při práci s methyldichlorarsinem CH 3 AsCl 2 se otrávil natolik, že upadl na podlahu laboratoře a ztratil vědomí. Až nouzová pomoc F.A. Kekuleho (1829–1896), který oběť vytáhl na čerstvý vzduch, umožnila předejít katastrofě. Bayer musel strávit několik dní v posteli. Kůže na jeho tváři byla červená a velmi zanícená.
Německý chemik A. Fischer stejně jako Kekula zachránil svého zaměstnance J. Tafela před blízkou smrtí poté, co byl otráven parami akroleinu.
Při práci v Meyerově laboratoři v Göttingenu se v roce 1885 slavný ruský chemik N.D. Zelinsky (1861–1953) vážně otrávil 2,2"-dichlordiethylsulfidem ClCH 2 CH 2 –S–CH 2 CH 2 Cl. Na rukou se mu vytvořily puchýře , obličej a tělo. Vědec byl nucen strávit několik měsíců v nemocnici. Látka, kterou dostal, byla následně použita Němci v roce 1917 v oblasti Ypres, poté byla nazvána „hořčičný plyn“.
L.Yu. Meyer (1830–1895), který na svých přednáškách rád demonstroval výbuch směsi acetylenu a vzduchu, byl v roce 1884 vážně zraněn. Jednou při takové demonstraci došlo k výbuchu takové síly, že zničil veškeré zařízení a zranil samotného experimentátora.
Nádoba obsahující brom kdysi explodovala v rukou ruského chemika S.V. Lebeděva (1874–1934). Úlomky skla a cákance bromu dopadly na vědcovy ruce a obličej, zranily je a způsobily vážné popáleniny. Navzdory včasné pomoci zůstaly některé úlomky v Lebeděvově těle a byly chirurgicky odstraněny až o tři roky později.
Když mluvíme o explozích v laboratoři, nelze nezmínit německého chemika Justuse Liebiga (1803–1873), kterého exploze provázely téměř po celou dobu jeho studia chemie, počínaje dětstvím, a byly příčinou mnoha jeho životní potíže.
Poté, co byl Justus vyloučen ze školy kvůli výbuchu, ke kterému došlo přímo ve třídě, jeho otec zařídil, aby se Liebig stal lékárnickým učedníkem. Ani zde se ale dlouho nezdržel. Po silné explozi, která odnesla střechu podkroví, ve kterém 15letý chlapec prováděl pokusy s rtuťnatým fulminátem (rtuťový fulminát) ![]() , Justus byl vyloučen z lékárny.
, Justus byl vyloučen z lékárny.
Liebig chtěl ve vyšším věku výbušné stříbro nějak rozložit sulfidem amonným. Jakmile však první kapka roztoku spadla do šálku stříbrného fulminátu, ozval se ohlušující výbuch. Liebiga hodili na záda, na dva týdny ztratil sluch a málem oslepl. Justus, již zralý vědec, kdysi na přednášce předvedl spalování par sirouhlíku v oxidu dusíku (II). Najednou došlo k silné explozi, úlomky baňky, kde k reakci došlo, zasypaly všechny přítomné. Liebig měl opět štěstí: největší úlomek zasáhl tabatěrku, kterou měl vědec v kapse.
Bohužel ne všichni chemici měli takové štěstí jako Liebig. Na následky otravy arsenem, který se při výbuchu retorty dostal do plic a jícnu, zemřel slavný mineralog a chemik, akademik petrohradské akademie věd I. G. Leman (1719–1767). Další ruský akademik N.P.Sokolov (1748–1795) zemřel na otravu fosforem a arsenem při studiu vlastností sloučenin těchto prvků. Další ruský chemik, bývalý nevolník, S. P. Vlasov (1789–1821) zemřel na následky otravy získané během chemického výzkumu.
Při explozi, ke které došlo při destilaci černouhelného dehtu, utrpěl anglický vědec Charles Mansfield (1819–1855) těžké popáleniny, na které o několik dní později zemřel.
V roce 1891 na hlavní dělostřelecké střelnici u Petrohradu při testování kyseliny pikrové (2,4,6-trinitrofenol-1)

exploze zabila řádného člena Ruské fyzikálně-chemické společnosti, soukromého učitele chemie ve Sboru Pages a Pavlovské vojenské školy, štábního kapitána gardového dělostřelectva S.V. Panpushko, autora první v Rusku „Sbírka problémů z chemie s vysvětlením jejich řešení“ a základní práce „Analýza střelného prachu“.
 |
Život talentované ruské vědkyně V.E. Bogdanovské (1867–1896), autorky „Základní učebnice chemie“ a řady románů a povídek, byl tragicky zkrácen. Při pokusu získat fosforový analog kyseliny kyanovodíkové explodovala ampule, jejíž sklo zranilo Bogdanovskou ruku. Na následky otravy toxickými látkami zemřela čtyři hodiny po výbuchu.
Již výše bylo zmíněno, jaké potíže vědcům přineslo studium a práce s látkami, jako je rtuť nebo chlór. Mezi jednoduchými látkami však badatelům dělal největší potíže fluor. Tento prvek se stal pro řadu chemiků z různých zemí skutečně osudným. O otravě fluorovodíkem G. Davy (1778–1829) již bylo napsáno. Francouzi J. Gay-Lussac, L. Thénard, E. Fremy a Angličan G. Gore si při pokusu o izolaci fluoru vážně podlomili zdraví, belgický chemik P. Layet zaplatil životem a francouzský vědec D. Nickles trpěl mučednictví. Pokusy získat fluor jeho izolací z fluoridů stříbra a olova, které podnikli angličtí chemici bratři Knoxové, skončily tragicky: George se stal invalidou a Thomas zemřel. Jiní vědci, kteří se pokusili izolovat tento prvek ve volné formě, také trpěli do té či oné míry.
 |
Teprve francouzskému vědci A. Moissanovi (1852–1907) se v roce 1886 podařilo to, co ostatní nedokázali. Poznamenáváme však, že pro něj řešení tohoto problému neprošlo beze stopy. Když Moissan oznámil svůj objev pařížské akademii věd, jedno z vědcových očí bylo zakryto černým obvazem.
Výše uvedené nehody se staly slavným chemikům. A kolik výbuchů a otrav se stalo mezi méně známými výzkumníky a začínajícími experimentátory! Kolik zranění, popálenin a zmrzačení bylo přijato!
Studium fenoménu radioaktivity přineslo vědcům také mnoho problémů. Záření je ze své podstaty životu nebezpečné. Ve velkých dávkách způsobuje vážné poškození tkání vedoucí k rychlé smrti těla a v malých dávkách může vést k rakovině nebo genetickým změnám.
Jedním z prvních, kdo se s účinky radioaktivního záření na tkáně živého organismu setkal, byl objevitel fenoménu radioaktivity, francouzský vědec A.A.Becquerel (1852–1908). Poté, co nějakou dobu nosil v kapse vesty zkumavku s radiovou solí, utrpěl v dubnu 1901 popáleninu kůže. Když o tom Becquerel vyprávěl Curies, zvolal: "Miluji radium, ale uráží mě to!"
Život anglického vědce W. Ramsaye (1852–1916) výrazně zkrátila práce s radiem, radonem a dalšími radioaktivními látkami. V roce 1915 vědec onemocněl rakovinou plic a zemřel rok po vážné operaci.
Práce s radioaktivními látkami měla silný dopad i na zdraví Marie Skłodowské-Curie (1867–1934). Nejprve podstoupila vážnou operaci ledvin, pak se jí prudce zhoršilo vidění a objevily se u ní problémy se sluchem. V roce 1920 v dopise své sestře napsala: „Moje vidění velmi zesláblo a pravděpodobně v tom není pomoci. Pokud jde o sluch, pronásleduje mě neustálý tinnitus, někdy velmi silný.“ V letech 1923 až 1930 Maria podstoupila čtyři operace očí, které jí nakonec zrak vrátily.
Sklodowska-Curie zemřela 4. července 1934 na akutní perniciózní anémii způsobenou degenerací kostní dřeně. V lékařské zprávě profesor Rego napsal: „Madame Curie lze považovat za jednu z obětí dlouhodobého nakládání s radioaktivními látkami, které její manžel a ona objevili.“
Sklodowska-Curie byla pohřbena se zvláštními opatřeními. Dřevěná rakev byla umístěna v olověné rakvi, která byla zase umístěna v jiné dřevěné. Když byly ostatky vynikajícího vědce přeneseny do Pantheonu v roce 1995, měření úrovně radiace vnitřní rakve ukázala, že byla 30krát vyšší než úroveň pozadí.
O Výše napsané příklady, i když je provázely velmi vážné důsledky, se stále týkaly především pouze samotných výzkumníků, kteří experimenty prováděli. Bohužel jsou známy případy, kdy při chemických pokusech byl počet obětí mnohem větší. „Černým dnem“ v dějinách chemie byl 27. květen 1920. V tento den došlo při demonstraci experimentů při vysokých teplotách na univerzitě v Münsteru (Německo) k silné explozi, v jejímž důsledku bylo deset studentů zabito a přes dvacet bylo zraněno.
A kolik lidí zemřelo na následky výbuchů v chemických závodech! Jednou z prvních takových nehod byl výbuch v továrně na střelný prach v Essonne v roce 1788, při kterém zemřelo několik lidí a francouzští chemici Berthollet a Lavoisier, kteří dorazili do továrny, přežili jen díky tomu, že se rozhodli prozkoumat přilehlou místnost. čas. Příčinou výbuchu byl pokus nahradit ve složení střelného prachu dusičnan draselný chlorečnanem draselným.
V roce 1848 v Le Bourget ve Francii vzlétl první závod na výrobu pyroxylinu - trinitrátu celulózy [C 6 H 7 O 2 (ONO 2) 3 ] n -.
3. září 1864 v poledne děsivá exploze srovnala se zemí továrnu na nitroglycerin C 3 H 5 (ONO 2) 3, která se nacházela nedaleko Stockholmu a patřila vynálezci dynamitu, švédskému inženýrovi Alfredu Nobelovi. V důsledku výbuchu zemřel Alfredův mladší bratr Oscar a také vynálezcův nejbližší přítel, chemik Hetzman.
V roce 1887 došlo v Anglii poblíž Manchesteru k silnému výbuchu v továrně na barvení, která používala sloučeniny kyseliny pikrové jako žlutou barvu.
Všechny tyto případy však nelze srovnávat s výbuchy, ke kterým došlo 6. prosince 1917 v chemické továrně v Halifaxu (Kanada), 21. září 1921 v továrně na hnojiva v Oppau (Německo) a 2. prosince 1984 v hod. závod na výrobu pesticidů v indickém městě Bhópál.
V prvním případě stál výbuch, ke kterému došlo v důsledku samorozkladu dusičnanu amonného, 3000 lidí, ve druhém zemřelo 560 lidí a více než 7500 zůstalo bez domova. Výbuch v Oppau byl tak silný, že nejen že zcela zničil všechny domy v samotném městě, ale poškodil i některé budovy 6 km od místa výbuchu. Tlaková vlna navíc rozbila sklo v domech vzdálených 70 km od elektrárny.
Výbuch v továrně na výrobu pesticidů v Bhópálu uvolnil do životního prostředí velké množství methylisokyanátu CH 3 –N=C=O, toxické látky se štiplavým zápachem a vysokou reaktivitou. V důsledku neštěstí zemřelo 2 352 lidí, 90 000 lidí se otrávilo a asi 150 000 lidí opustilo město v panice.
Připomeňme také tragédii, která se odehrála v červenci 1976 v Itálii. Kvůli havárii v chemické továrně ve vesnici Seveso nedaleko Milána se do atmosféry dostal dioxin

Jedná se o jeden z nejsilnějších jedů, jehož účinek je silnější než kyselina kyanovodíková, strychnin a jed kurare. Stovky lidí se otrávily a skončily v nemocnicích. Jejich kůže byla pokryta ekzémy, vředy a popáleninami, trpěli zvracením, žaludečními křečemi a nevolnostmi. Veškerá vegetace v okolí Seveso, včetně plodin, byla spálena jako při požáru a samotná půda se stala na desítky let nebezpečnou pro lidi i dobytek.
V U naprosté většiny výše uvedených nehod, ke kterým došlo v laboratořích nebo chemických závodech, byly tragédie pro výzkumníka nebo technologa překvapením. Vědec však často neměl po ruce žádné jiné organismy než své vlastní a dychtil rychle studovat vlastnosti nové látky, provedl na sobě experiment, obětoval své zdraví a někdy i život sám, aby pochopil pravdu. . Aby ospravedlnili své činy, takoví chemici tvrdili, že věda vyžaduje oběti, a pokračovali v nebezpečných experimentech, dokud mohli pracovat v laboratoři.
Připomeňme znovu K. Scheeleho, T. Lowitze, K. Klause, kteří určovali chuť chemických látek. Vzpomeňme na G. Davyho, D. Wodehouse, W. Cruikshanka, kteří zkoumali vliv plynů na vlastní tělo. Vzpomeňme na stovky dalších slavných i neznámých chemiků, kteří se podobným výzkumem zabývali. Zde je několik dalších příkladů z této oblasti.
Kdysi dávno francouzský přírodovědec 18. století. Jean François Pilâtre de Rosier se zajímal o otázku: co se stane, když vdechnete vodík? Vědec, který zpočátku necítil žádný účinek, se rozhodl ujistit se, zda vodík pronikl do plic. Aby to udělal, znovu vdechl plyn a pak ho vydechl do ohně svíčky. Ozval se ohlušující výbuch. "Myslel jsem, že mi vyletí všechny zuby spolu s kořeny," napsal později vědec o zážitku, který ho málem stál život.
Ve snaze prokázat bezpečnost aktivního uhlí pro tělo provedl Lovitz následující experiment. Spálil 100 gramů opia, což je silná droga, a pak všechno vzniklé dřevěné uhlí během dne snědl. Pro ty, kteří měli pochybnosti, Lovitz navrhl provést podobný experiment s jakýmkoli jiným rostlinným jedem.
Na rozdíl od Becquerela, který nešťastnou náhodou utrpěl popáleniny v důsledku působení radia na kůži, P. Curie (1859–1906) dobrovolně vystavil ruku této látce. Poté, co byl vystaven záření po dobu 10 hodin, jeho kůže nejprve zčervenala a pak se objevila rána, která se hojila déle než čtyři měsíce, s bílou jizvou, která přetrvávala několik let.
 |
Ramsay zažil účinky injekcí radioaktivního radonu. Navzdory skutečnosti, že podle Ramsayho jsou takové injekce účinným prostředkem proti rakovině, zřejmě byly příčinou vědcovy brzké smrti.
Americký fyzikální chemik G. Ury (1893–1981) na sebe, objevitele deuteria, zkoumal i vliv těžké vody. Jednoho dne dokonce vypil plnou sklenici těžké vody. Naštěstí pro něj tento riskantní experiment prošel bez následků.
Jak je ze všeho výše patrné, nebezpečí při pokusech a ztráta zdraví v důsledku chemických pokusů byly v minulosti považovány za téměř povinné atributy práce chemika a byly jakoby předem plánovány. Tuto myšlenku v koncentrované podobě vyjadřují slova velkého německého chemika Liebiga, který jednou, když dával pokyny mladému Kekulovi, řekl: „Chceš-li se stát skutečným chemikem, musíš obětovat své zdraví. V naší době každý, kdo si při studiu chemie nezničí zdraví, v této vědě ničeho nedosáhne.“ Z toho plyne, že Liebig nejen že nedbal na zachování svého zdraví, ale nemyslel ani na zachování zdraví lidí kolem sebe. Následující příklad je v tomto ohledu zvláště názorný.
Poté, co dostal bezvodou kyselinu mravenčí a na vlastní kůži se přesvědčil, že kyselina způsobuje popáleniny, začal Liebig chodit po laboratoři a aby svůj objev jasně demonstroval, začal studentům pálit ruce. Liebig sám měl na tváři velkou bublinu od cákání kyseliny, ale nevěnoval tomu žádnou pozornost. Největší porci kyseliny dostal Liebigův kolega, slavný německý fyziolog a biochemik K. Vogt (1817–1895), který si Liebig bez stínu rozpaků aplikoval na ruku. Důsledkem tohoto ukvapeného experimentu byla bílá jizva, která zůstala Vogtovi po zbytek jeho života.
Od té doby proteklo pod mostem hodně vody. V naší době pohled na problémy udržení zdraví při hodinách chemie ve srovnání s 18. a 19. stoletím. se dramaticky změnil. Málokoho teď napadne ochutnávat neznámé látky nebo si pálit ruce kyselinami. Nikdo nemá touhu ničit si zdraví. Chemici se naopak snaží v moderní laboratoři vytvořit podmínky, které co nejvíce zajistí jejich bezpečnost.
Ale zkušenosti chemiků z minulosti neprošly beze stopy. Obětovali se pro pravdu a pomocí vlastních zkušeností varovali budoucí generace vědců před nebezpečím práce s tou či onou látkou. Na tomto základě byla zdokonalována opatření na ochranu před toxickými, výbušnými a radioaktivními látkami, vyvinuto laboratorní vybavení a byly vyvinuty bezpečnější metody syntézy a analýzy.
V dnešní době, i přes vysokou toxicitu a nebezpečnost mnoha látek, chemici dokázali, že práce s nimi může být naprosto neškodná. V tom jim pomáhají promyšlená opatření: silná trakce, ochranné materiály (brýle, rukavice, zástěry, plynové masky, obrazovky), používání manipulátorů a dalších ochranných prostředků. To vše dohromady nám umožňuje vyhnout se škodlivým účinkům toxických látek na organismy chemiků a tím jim vytváří podmínky pro dlouhý a plodný život.
APLIKACE
Stůl
Nehody zahrnující výzkumné chemiky
| Příjmení vědce | Roky života | Země | Příčina zranění (otrava nebo výbuch) |
|---|---|---|---|
Otrava |
|||
| T. Paracelsus | 1493–1541 | Německo | Rtuť a její sloučeniny |
| I.Glauber | 1604–1670 | Německo | Kyselina chlorovodíková, sloučeniny rtuti a antimonu |
| R.Boyle | 1627–1691 | Anglie | Fosfor a jeho sloučeniny |
| I. Newton | 1643–1727 | Anglie | Rtuť a její sloučeniny |
| K.Scheele | 1742–1786 | Švédsko | Kyselina kyanovodíková, chlór, sloučeniny arsenu a rtuti |
| W. Kruikshank | 1745–1810 | Anglie | Oxid uhelnatý, fosgen, chlór |
| K. Berthollet | 1748–1822 | Francie | Chlór, čpavek, sirovodík, kyanovodík |
| N. Sokolov | 1748–1795 | Rusko | Fosfor, arsen |
| T. Lovitz | 1757–1804 | Rusko | Sloučeniny rtuti, chloru, stroncia |
| D.Woodhouse | 1770–1809 | Anglie | Kysličník uhelnatý |
| L. Tenar | 1777–1857 | Francie | Sublimát, fluorovodík |
| J. Gay-Lussac | 1778–1850 | Francie | Fluorovodík |
| G. Davy | 1778–1829 | Anglie | Oxid uhelnatý, metan, fluorovodík |
| J. Berzelius | 1779–1848 | Švédsko | Selenid vodíku |
| K.Klaus | 1796–1864 | Rusko | Sloučeniny osmia, ruthenium |
| R. Bunsen | 1811–1899 | Německo | Sloučeniny arsenu |
| E. Fremy | 1814–1894 | Francie | Fluorovodík |
| A.Bayer | 1835–1917 | Německo | methyldichlorarsin |
| N. Zelinského | 1861–1953 | Rusko | 2,2"-dichlordiethylsulfid |
| E. Fisher | 1852–1919 | Německo | fenylhydrazin |
| W. Ramsay | 1852–1916 | Anglie | Radium, radon |
| Yu.Tafel | 1862–1918 | Německo | akrolein |
| M. Sklodowská-Curie | 1867–1934 | Francie | Radium, polonium |
Výbuchy |
|||
| I.Leman | 1719–1767 | Rusko | Arsen |
| K. Berthollet | 1748–1822 | Francie | Bertholetova sůl |
| G. Davy | 1778–1829 | Anglie | Alkalické kovy |
| L. Tenar | 1777–1857 | Francie | KOH a Fe |
| J. Gay-Lussac | 1778–1850 | Francie | KOH a Fe |
| P. Dulong | 1785–1838 | Francie | Chlorid dusičitý |
| Yu, Liebigu | 1803–1873 | Německo | Rtuťový fulminát, stříbrný fulminát |
| R. Bunsen | 1811–1899 | Německo | Sloučeniny arsenu |
| S. Wurtz | 1817–1884 | Francie | PCl3 a Na |
| Ch.Mansfield | 1819–1855 | Anglie | Těkavá frakce černouhelného dehtu |
| L. Meyer | 1830–1895 | Německo | Směs acetylenu a vzduchu |
| V. Bogdanovská | 1867–1896 | Rusko | Fosfin |
REFERENCE
Manolov K. Skvělí chemici. T. 1–2. M.: Mir, 1985;
Volkov D.N., Vonsky E.V., Kuzněcovová G.I. Vynikající chemici světa. M.: Vyšší škola, 1991; Stepin B.D., Alikberová L.Yu. Kniha o chemii pro domácí čtení. M.: Khimiya, 1994;
Ključevič A.S. Karl Karlovich Klaus. Kazan: Kazan University Publishing House, 1972;
Figurovsky N.A., Ushakova N.N.. Tovij Jegorovič Lovitz. M.: Nauka, 1988;
Mogilevskij B.L.Žijte v nebezpečí! Příběh velkého chemika Humphryho Davyho. M.: Dětská literatura, 1970;
Curie E. Marie Curie. M.: Atomizdat, 1973;
Krasnogorov V. Justus Liebig. M.: Znanie, 1980;
Trifonov D.N., Trifonov V.D. Jak byly objeveny chemické prvky. M.: Vzdělávání, 1980; Soloveichik S. Neopatrnost, která stála život. Chemie a život, 1966, č. 6, s. 29;
Děmidov V.I.„Horký med“ – melinitida. Chemie a život, 1974, č. 8, s. 61;
Kolchinsky A.G. Lekce z TBC. Chemie a život, 1990, č. 2, s. 79;
Zyablov V. Dvě legendy o Tobiasi Lowitzovi. Chemie a život, 1977, č. 4, s. 79.
Význam studie: Voda je jednou z nejstarších látek na planetě. Mnoho vědců se v minulosti pokusilo rozluštit některé jeho vlastnosti, rozplétají je nyní i v blízké budoucnosti. Protože voda je nejzáhadnější látka. Význam studie: Voda je jednou z nejstarších látek na planetě. Mnoho vědců se v minulosti pokusilo rozluštit některé jeho vlastnosti, rozplétají je nyní i v blízké budoucnosti. Protože voda je nejzáhadnější látka. Účel výzkumné činnosti: Studovat vlastnosti vody z pohledu chemie a fyziky. Účel výzkumné činnosti: Studovat vlastnosti vody z pohledu chemie a fyziky.
Cíle: 1. studium vody jako látky; 2. zvážit historii studia vody; 3. zvážit jeho chemické a fyzikální vlastnosti; 4. studovat různé studie vědců; 5. rozšířit své obzory; Cíle: 1. studium vody jako látky; 2. zvážit historii studia vody; 3. zvážit jeho chemické a fyzikální vlastnosti; 4. studovat různé studie vědců; 5. rozšířit své obzory; Problém: Mnoho lidí si myslí, že voda již byla studována. Já zase chci dokázat, že tomu tak není.








Podle charakteristiky původu, složení nebo aplikace rozlišují mimo jiné: Měkkou vodu a tvrdou vodu podle obsahu kationtů vápníku a hořčíku Podle izotopů molekuly: Lehká voda (složením téměř shodná s běžnou vodou ) Těžká voda (deuterium) Supertěžká voda (tritium) Sladká voda Dešťová voda Mořská voda Pitná voda Voda z vodovodu Destilovaná voda a deionizovaná voda atd.


Mnoho lidí je zvyklých si myslet, že kapaliny, včetně vody, nemají tvar. Ale to není pravda. Jejich přirozený tvar je koule. Obvykle gravitace brání kapalině v tom, aby získala tento tvar, a kapalina se buď šíří v tenké vrstvě po povrchu, pokud je nalévána bez nádoby, nebo má tvar nádoby, pokud je do ní nalévána. Tím, že je uvnitř jiné kapaliny se stejnou hustotou, kapalina podle Archimédova zákona „ztrácí“ svou váhu: zdá se, že nic neváží, gravitace na ni nepůsobí – a pak kapalina nabývá svého přirozeného kulovitého tvaru.


Překvapivě rozmanité jsou také projevy povrchové vrstvy kapaliny v přírodě a technice. Sbírá vodu do kapiček, můžeme si díky ní vynutit mýdlovou bublinu a psát perem. Povrchové napětí hraje důležitou roli ve fyziologii našeho těla. Používá se také v kosmické technologii. Proč se povrch kapaliny chová jako natažený elastický film?

Zjistil jsem, že voda má tvar koule. A tak jsem se rozhodl blíže podívat na tvar kapky. Například kapka kapaliny není téměř nikdy koule, ačkoli koule má nejmenší povrch ze všech obrazců pro daný objem. Když kapka spočívá na nehybném vodorovném povrchu, zploští se. Kapka padající do vzduchu má také složitý tvar. A jen kapka beztíže nabývá dokonalého kulového tvaru. Svou Platónovu metodu, kterou jsem studoval tvar kapaliny, jsem aplikoval i na studium různých jevů. Studoval například proces vzniku a oddělení kapky kapaliny na konci trubice. Obvykle, bez ohledu na to, jak pomalu lidé zvětšují kapku, se z tuby oddělí tak rychle, že oko nemůže sledovat podrobnosti tohoto procesu.



Další úžasnou vlastností je, že pomocí vodního paprsku můžete úspěšně zesílit různé zvuky. Toto neobvyklé zařízení vyrobil Američan Alexander Bell, který je známější jako jeden z vynálezců telefonu. Nejprve se seznámím s vlastnostmi jeho „zesilovače“ - vodního paprsku. Pokud vyvrtáte do dna nádoby s vodou malý kulatý otvor, všimnete si, že proud z něj vytékající se skládá ze dvou částí s rozdílnými vlastnostmi. Horní část potoka je průhledná a tak nehybná, že vypadá jako sklo.


Jak se vzdaluje od zdroje, ztenčuje se a v místě největšího smršťování začíná spodní část, tvarově proměnlivá a neprůhledná. Na první pohled působí tato část toku, stejně jako ta horní, souvislá. Někdy jím však můžete rychle projet prstem, aniž byste jej namočili. Bell k tomuto závěru dospěl díky práci dvou vědců.

Bell k tomuto závěru dospěl díky práci dvou vědců. Jedním z nich byl francouzský fyzik Felix Savard, který provedl podrobnou studii vlastností vodního paprsku a došel k závěru, že v nejužším místě přestává být vodní paprsek souvislý a rozpadá se na samostatné kapky. Druhým byl anglický fyzik John Tyndall, který zopakoval Savartův experiment ve své laboratoři. Podařilo se mu vytvořit proudnici, jejíž průhledná část dosahovala délky asi 90 stop (27,4 m). pod vlivem zvuku varhanní píšťaly náležité čistoty a střední síly se tato průhledná žíla zakalila a rozpadla se na obrovské množství vodních kapek.

Podíval jsem se blíže na Bellův přístroj. Jedná se o kovovou trubku s pájenou trubkou, ale s připojeným trychtýřem. Spodní konec této trubky je namontován na stojanu a horní konec je pokryt kusem elastické pryžové membrány, připevněné k trubce závitem. Z Tyndallových pokusů jsem se dozvěděl, že když proud vody vnikne do bazénu, jeho spodní část, která se rozpadá na kapky, produkuje hluk. Pokud horní, pevná část proudu vstoupí do vody, pak tiše vtéká do bazénu. Podobný experiment lze provést s kusem lepenky. Pokud se tedy list lepenky, na který dopadá proud vody, zvedne ke svému zdroji, dopady kapek budou slyšet stále slabší a po dosažení bodu zlomu nebudou slyšet vůbec.

Membrána v mikrofonu Bell hraje roli stejného listu lepenky. Díky rezonátoru, což je elektronka, a klaksonu je však každý tichý kapkový úder slyšet mnohem lépe. Kapky dopadající na pryžovou membránu tak v místnosti působí dojmem slabých úderů kladiva o kovadlinu. Pokud ale přiložíte stopku vibrační ladičky, proud se okamžitě rozpadne na kapky, které při dopadu na membránu „zazpívají“ natolik, že si budete chtít zacpat uši. Bell to samozřejmě ve svém vynálezu nepoužil.

Rozhodl jsem se zjistit, jaké další studie vědci provedli s vodou, a zjistil jsem, že vědci souhlasí s tím, že voda je jedním z nejobtížnějších předmětů studia, protože voda v první řadě vždy obsahuje nečistoty a že má kooperativní povahu. interakce jeho molekul. Přezkoumal jsem studie Whitinga, G. Stewarta, S.W. Zenina

Závěr: Provedl jsem různé typy experimentů. Díky tomu jsem se naučil spoustu nových věcí. Například, že jakákoli kapalina, včetně vody, má kulovitý tvar, Alexander Bell použil vodu jako vodní mikrofon a mnoho dalšího. Voda mi ale stále zůstává záhadou, protože ještě není plně prozkoumána. Nebo by to možná nemělo být úplně studováno, možná vytvořeno přírodou, voda se nechce řešit? Na tuto otázku nikdo nezná odpověď.


) provedla studii o využití vysokoenergetických sloučenin dusík-kyslík v organické syntéze. Energii obsaženou v těchto nestabilních sloučeninách lze využít k vybudování nových, stabilnějších chemických vazeb. Pomocí tohoto přístupu bylo možné získat biologicky aktivní látky obsahující dusík včetně léčiv. Výzkum podporován grant Ruská vědecká nadace (RSF). Článek byl nedávno zveřejněno v německém časopise Synthesis.
Vědci zkoumali vlastnosti nitronátů. Kromě uhlovodíkového řetězce obsahují tyto organické sloučeniny nestabilní chemickou skupinu sestávající ze dvou atomů kyslíku a jednoho atomu dusíku. Při zahřívání se taková nestabilní skupina rozkládá, přičemž se uvolňuje velké množství energie, proto jsou tyto sloučeniny obvykle považovány za vysokoenergetické (výbušné).
„V našem výzkumu nevyužíváme vysokou energii obsaženou v nestabilních sloučeninách dusíku a kyslíku ne za účelem ničení, ale pro tvorbu na molekulární úrovni. Pomocí řízených chemických procesů je možné dosáhnout destrukce (zničení) dusíko-kyslíkového fragmentu tak, že uvolněná energie je využita k budování nových stabilních chemických vazeb v molekulách,“ vysvětluje jeden z autorů studie Kandidát chemických věd, vedoucí vědecký pracovník Ústavu organické chemie Ruské akademie věd.
Uhlovodíky podléhají malému počtu reakcí, to znamená, že jsou chemicky relativně inertní. V uhlovodíkovém řetězci je obtížné nahradit jeden z uhlíků jiným atomem (například kyslíkem nebo dusíkem) nebo „sestavit“ několik malých molekul do složité struktury. Pokud molekuly „aktivujete“ nitroskupinou a získáte nitronát, lze tyto úkoly snadno splnit.
Většina nitronátů je nestabilních pouze při zvýšených teplotách, takže práce s nimi při pokojových teplotách je poměrně bezpečná. Metody použité ve studii zahrnují použití Lewisových kyselin a sloučenin přechodných kovů v reakcích. Lewisovy kyseliny jsou široce používány jako katalyzátory - látky, které mnohonásobně urychlují chemické reakce. V této studii byly Lewisovy kyseliny použity k aktivaci sloučenin při teplotě místnosti nebo nižší. Katalyzátory a experimentální podmínky se lišily v závislosti na konkrétní reakci a cílovém produktu.
Je důležité, že díky použití nitronátů jako klíčových meziproduktů lze získat pouze jeden optický izomer (nebo stereoizomer) syntetizované sloučeniny. Mnoho komplexních organických molekul má stereoizomery - molekuly, které jsou identické v chemickém složení a struktuře, ale liší se od sebe uspořádáním skupin atomů. Pokud má molekula jeden atom uhlíku, ke kterému jsou vázány čtyři různé substituenty, může mít tato molekula dva optické izomery – dvě formy, které jsou navzájem zrcadlovými obrazy, jako levá a pravá rukavice.
Obvykle mají optické izomery prakticky stejné fyzikální a chemické vlastnosti, ale biologická aktivita velmi závisí na tom, který izomer vstoupí do těla. Jsme například schopni ochutnat rozdíl mezi sladkou náhražkou cukru aspartamem a jeho hořkým stereoizomerem, i když se liší pouze směrem, kterým části molekuly směřují. Buňky vnímají všechny látky vstupující do těla pomocí receptorů. Jedná se o velké, obvykle proteinové molekuly, které se nacházejí na vnější části buněčné membrány. Aby buňka reagovala na přítomnost látky, musí se vázat na receptorové proteiny, což jsou zase také asymetrické molekuly. „Špatný“ optický izomer nevyhovuje receptorovému proteinu ze stejného důvodu, z jakého levá rukavice nesedí na pravou ruku. To je velmi důležité při výrobě léků.
Při konvenční chemické syntéze se obě formy nejčastěji získávají ve stejném množství. Pro získání pouze jednoho optického izomeru je nutné použít metody asymetrické katalýzy. A právě zde nacházejí uplatnění systémy dusík-kyslík. Reakce s nitronáty za použití určitých katalyzátorů umožňují získat biologicky aktivní sloučeniny stereosměrně, to znamená ve formě jednoho optického izomeru nezbytného pro tělo.
Použití nitronátů již umožnilo získat nové biologické látky obsahující dusík a také zefektivnit proces tvorby již známých sloučenin. Vědci například syntetizovali nové inhibitory fosfodiesterázy-4. Tyto látky jsou perspektivním lékem na chronickou obstrukční plicní nemoc – omezení proudění vzduchu v dýchacích cestách v důsledku zánětu plicní tkáně. Použití nitronátů umožňuje snížit počet fází výroby farmaceutických látek, jako je baklofen a fenibut, které se již používají jako léčiva. Také se hledají účinnější náhražky již známých biologicky aktivních látek.
Skupina vědců z Ústavu organické chemie RAS pracuje na několika úkolech. Jednak se jedná o rozšíření škály transformací a palety výsledných produktů. Vědci se snaží využít ty reakce, které již byly objeveny, pro syntézu existujících prakticky významných sloučenin a jejich analogů. Za druhé jsou studovány základní rysy chování nitronátů, díky nimž lze vytvářet nové metody organické syntézy.
„Doufáme, že metodika, kterou vyvíjíme, zaujme v budoucnu své právoplatné místo v aplikované organické syntéze,“ uzavírá Alexey Sukhorukov.